Розрахунок кількості теплоти, необхідної для нагрівання тіла або виділеного ним при охолодженні. Кількість теплоти. Рівняння теплового балансу
1. Зміна внутрішньої енергії шляхом роботи характеризується величиною роботи, тобто. робота є мірою зміни внутрішньої енергії у цьому процесі. Зміна внутрішньої енергії тіла при теплопередачі характеризується величиною, яка називається кількістю теплоти.
Кількість теплоти називається зміна внутрішньої енергії тіла в процесі теплопередачі без виконання роботи.
Кількість теплоти позначають буквою (Q). Оскільки кількість теплоти є мірою зміни внутрішньої енергії, його одиницею є джоуль (1 Дж).
При передачі тілу деякої кількості теплоти без роботи його внутрішня енергія збільшується, якщо тіло віддає певну кількість теплоти, його внутрішня енергія зменшується.
2. Якщо в дві однакові судини налити в один 100 г води, а в іншій 400 г при одній і тій же температурі і поставити їх на однакові пальники, то раніше закипить вода в першій посудині. Таким чином, що більша маса тіла, то більша кількість теплоти потрібна йому для нагрівання. Те саме і з охолодженням: тіло більшої маси при охолодженні віддає більшу кількість теплоти. Ці тіла зроблені з однієї і тієї ж речовини і нагріваються вони або охолоджуються на те саме число градусів.
3. Якщо тепер нагрівати 100 р води від 30 до 60 °З, тобто. на 30 °С, та був до 100 °З, тобто. на 70 °С, то в першому випадку на нагрівання піде менше часу, ніж у другому, і, відповідно, на нагрівання води на 30 °С, буде витрачено менше теплоти, ніж на нагрівання води на 70 °С. Таким чином, кількість теплоти прямо пропорційно різниці кінцевої ((t_2\,^\circ C) \) і початкової \((t_1\,^\circ C) \) температур: (Q\sim(t_2- t_1) \) .
4. Якщо тепер в один посуд налити 100 г води, а в інший такий самий посуд налити трохи води і покласти в неї таке металеве тіло, щоб його маса і маса води становили 100 г, і нагрівати судини на однакових плитках, то можна помітити, що в посудині, в якій знаходиться тільки вода, температура буде нижчою, ніж у тій, у якій знаходяться вода та металеве тіло. Отже, щоб температура вмісту в обох судинах була однаковою, потрібно воді передати більшу кількість теплоти, ніж воді. металевому тілу. Таким чином, кількість теплоти, необхідне для нагрівання тіла, залежить від роду речовини, з якої це тіло зроблено.
5. Залежність кількості теплоти, необхідної для нагрівання тіла, від роду речовини характеризується фізичною величиною, яка називається питомою теплоємністюречовини.
Фізична величина, що дорівнює кількості теплоти, яку необхідно повідомити 1 кг речовини для нагрівання його на 1 ° С (або на 1 К), називається питомою теплоємністю речовини.
Таку кількість теплоти 1 кг речовини віддає при охолодженні на 1 °С.
Питома теплоємність позначається буквою (c). Одиницею питомої теплоємності є 1 Дж/кг °З чи 1 Дж/кг До.
Значення питомої теплоємності речовин визначають експериментально. Рідини мають більшу питому теплоємність, ніж метали; найбільшу питому теплоємність має вода, дуже маленьку питому теплоємність має золото.
Питома теплоємність свинцю 140 Дж/кг. Це означає, що для нагрівання 1 кг свинцю на 1 °С необхідно витратити кількість теплоти 140 Дж. Така сама кількість теплоти виділиться при охолодженні 1 кг води на 1 °С.
Оскільки кількість теплоти дорівнює зміні внутрішньої енергії тіла, можна сказати, що питома теплоємність показує, наскільки змінюється внутрішня енергія 1 кг речовини за зміни її температури на 1 °З. Зокрема, внутрішня енергія 1 кг свинцю при нагріванні на 1 °С збільшується на 140 Дж, а при охолодженні зменшується на 140 Дж.
Кількість теплоти \(Q \) , необхідне для нагрівання тіла масою \(m \) від температури \((t_1\,^\circ C) \) до температури \((t_2\,^\circ C) \) , дорівнює добутку питомої теплоємності речовини, маси тіла та різниці кінцевої та початкової температур, тобто.
\[ Q=cm(t_2()^\circ-t_1()^\circ) \]
По цій же формулі обчислюється і кількість теплоти, яку тіло віддає при охолодженні. Тільки цьому випадку від початкової температури слід відібрати кінцеву, тобто. від більшого значення температури відібрати менше.
6. Приклад розв'язання задачі. У склянку, що містить 200 г води за температури 80 °С, налили 100 г води при температурі 20 °С. Після цього в посудині встановилася температура 60 °С. Яку кількість теплоти одержала холодна вода та віддала гаряча вода?
При розв'язанні задачі необхідно виконувати таку послідовність дій:
- записати коротко умову завдання;
- перевести значення величин у СІ;
- проаналізувати завдання, встановити, які тіла беруть участь у теплообміні, які тіла віддають енергію, а які одержують;
- вирішити задачу в загальному вигляді;
- виконати обчислення;
- проаналізувати отриману відповідь.
1. Умова задачі.
Дано:
(m_1 \) = 200 г
(m_2 \) = 100 г
(t_1 \) = 80 ° С
(t_2 \) = 20 ° С
? (t \) = 60 ° С
______________
? (Q_1 \) -? ? (Q_2 \) -?
(c_1 \) = 4200 Дж / кг · ° С
2. СІ:? (m_1 \) = 0,2 кг; (m_2 \) = 0,1 кг.
3. Аналіз завдання. У задачі описаний процес теплообміну між гарячою та холодною водою. Гаряча водавіддає кількість теплоти \ (Q_1 \) і охолоджується від температури \ (t_1 \) до температури \ (t \). Холодна водаотримує кількість теплоти \ (Q_2 \) і нагрівається від температури \ (t_2 \) до температури \ (t \).
4. Розв'язання задачі у загальному вигляді. Кількість теплоти, віддана гарячою водою, обчислюється за формулою: (Q_1 = c_1m_1 (t_1-t) \).
Кількість теплоти, одержане холодною водою, обчислюється за формулою: (Q_2=c_2m_2(t-t_2)).
5.
Обчислення.
(Q_1 \) = 4200 Дж / кг · ° С · 0,2 кг · 20 ° С = 16800 Дж
\(Q_2 \) = 4200 Дж/кг · ° С · 0,1 кг · 40 ° С = 16800 Дж
6. У відповіді отримано, що кількість теплоти, віддана гарячою водою, дорівнює кількості теплоти, отриманої холодною водою. При цьому розглядалася ідеалізована ситуація і не враховувалося, що деяка кількість теплоти пішла на нагрівання склянки, в якій знаходилася вода, та навколишнього повітря. Насправді кількість теплоти, віддане гарячою водою, більше, ніж кількість теплоти, отримане холодною водою.
Частина 1
1. Питома теплоємність срібла 250 Дж/(кг · °С). Що це означає?
1) при охолодженні 1 кг срібла на 250 °С виділяється кількість теплоти 1 Дж
2) при остиганні 250 кг срібла на 1 °С виділяється кількість теплоти 1 Дж
3) при остиганні 250 кг срібла на 1 °С поглинається кількість теплоти 1 Дж
4) при охолодженні 1 кг срібла на 1 °С виділяється кількість теплоти 250 Дж
2. Питома теплоємність цинку 400 Дж/(кг · °С). Це означає, що
1) при нагріванні 1 кг цинку на 400 ° С його внутрішня енергія збільшується на 1 Дж
2) при нагріванні 400 кг цинку на 1 °С його внутрішня енергія збільшується на 1 Дж
3) для нагрівання 400 кг цинку на 1 ° С його необхідно витратити 1 Дж енергії
4) при нагріванні 1 кг цинку на 1 °С його внутрішня енергія збільшується на 400 Дж
3. При передачі твердому тілумасою кількості теплоти (Q) температура тіла підвищилася на (Delta t ^ circ). Який із наведених нижче виразів визначає питому теплоємність речовини цього тіла?
1) \(\frac(m\Delta t^\circ)(Q) \)
2) \(\frac(Q)(m\Delta t^\circ) \)
3) \(\frac(Q)(\Delta t^\circ) \)
4) \ (Qm \ Delta t ^ \ circ \)
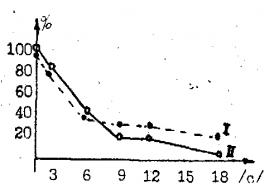
4. На малюнку наведено графік залежності кількості теплоти, необхідної для нагрівання двох тіл (1 та 2) однакової маси, від температури. Порівняйте значення питомої теплоємності (\(c_1 \) і (c_2 \)) речовин, з яких виготовлені ці тіла.

1) (c_1 = c_2 \)
2) (c_1> c_2 \)
3) \(c_1
5. На діаграмі представлені значення кількості теплоти, переданого двом тілам рівної маси при зміні їхньої температури на те саме число градусів. Яке співвідношення для питомих теплоємностей речовин, з яких виготовлені тіла, є вірним?

1) \(c_1 = c_2 \)
2) \(c_1 = 3c_2 \)
3) \(c_2 = 3c_1 \)
4) \(c_2=2c_1 \)
6. На малюнку представлений графік залежності температури твердого тіла від відданої кількості теплоти. Маса тіла – 4 кг. Чому дорівнює питома теплоємність речовини цього тіла?

1) 500 Дж/(кг · °С)
2) 250 Дж/(кг · °С)
3) 125 Дж/(кг · °С)
4) 100 Дж/(кг · °С)
7. При нагріванні кристалічної речовини масою 100 г вимірювали температуру речовини та кількість теплоти, повідомлену речовину. Дані вимірів подали у вигляді таблиці. Вважаючи, що втрати енергії можна знехтувати, визначте питому теплоємність речовини в твердому стані.
1) 192 Дж/(кг · °С)
2) 240 Дж/(кг · °С)
3) 576 Дж/(кг · °С)
4) 480 Дж/(кг · °С)
8. Щоб нагріти 192 г молібдену на 1 К, потрібно передати йому кількість теплоти 48 Дж. Чому дорівнює питома теплоємність цієї речовини?
1) 250 Дж/(кг · К)
2) 24 Дж/(кг · К)
3) 4·10 -3 Дж/(кг · К)
4) 0,92 Дж/(кг · К)
9. Яка кількість теплоти потрібна для нагрівання 100 г свинцю від 27 до 47 °С?
1) 390 Дж
2) 26 кДж
3) 260 Дж
4) 390 кДж
10. На нагрівання цеглини від 20 до 85 °С витрачено таку ж кількість теплоти, як для нагрівання води такої ж маси на 13 °С. Питома теплоємність цегли дорівнює
1) 840 Дж/(кг · К)
2) 21000 Дж/(кг · К)
3) 2100 Дж/(кг · К)
4) 1680 Дж/(кг · К)
11. З переліку наведених нижче висловлювань виберіть два правильні та запишіть їх номери в таблицю.
1) Кількість теплоти, яке тіло отримує при підвищенні його температури на деяке число градусів, дорівнює кількості теплоти, яку це тіло віддає при зниженні температури на таке ж число градусів.
2) При охолодженні речовини її внутрішня енергія збільшується.
3) Кількість теплоти, яку речовина отримує при нагріванні, йде головним чином збільшення кінетичної енергії його молекул.
4) Кількість теплоти, яку речовину отримує при нагріванні, йде головним чином на збільшення потенційної енергії взаємодії його молекул
5) Внутрішню енергію тіла можна змінити, лише повідомивши йому деяку кількість теплоти
12. У таблиці представлені результати вимірювань маси (m), зміни температури (Delta t) і кількості теплоти (Q), що виділяється при охолодженні циліндрів, виготовлених з міді або алюмінію.

Які твердження відповідають результатам проведеного експерименту? Із запропонованого переліку оберіть два правильні. Вкажіть їхні номери. На підставі проведених вимірювань можна стверджувати, що кількість теплоти, що виділяється при охолодженні,
1) залежить від речовини, з якої виготовлений циліндр.
2) не залежить від речовини, з якої виготовлений циліндр.
3) збільшується зі збільшенням маси циліндра.
4) збільшується зі збільшенням різниці температур.
5) питома теплоємність алюмінію в 4 рази більша, ніж питома теплоємність олова.
Частина 2
C1.Тверде тіло масою 2 кг поміщають у піч потужністю 2 кВт та починають нагрівати. На малюнку зображено залежність температури цього тіла від часу нагрівання (tau). Чому дорівнює питома теплоємність речовини?

1) 400 Дж/(кг · °С)
2) 200 Дж/(кг · °С)
3) 40 Дж/(кг · °С)
4) 20 Дж/(кг · °С)
Відповіді


У фокусі уваги нашої статті – кількість теплоти. Ми розглянемо поняття внутрішньої енергії, яка трансформується за зміни цієї величини. А також покажемо деякі приклади застосування розрахунків у людській діяльності.
Теплота
З будь-яким словом рідної мови кожна людина має свої асоціації. Вони визначаються особистим досвідом та ірраціональними почуттями. Що зазвичай здається при слові «теплота»? М'яка ковдра, батарея центрального опалення, що працює взимку, перше сонячне світло навесні, кіт. Або погляд матері, втішне слово друга, вчасно виявлену увагу.
Фізики мають на увазі під цим конкретний термін. І дуже важливий, особливо в деяких розділах цієї складної, але цікавої науки.

Термодинаміка
Розглядати кількість теплоти у відриві від найпростіших процесів, на які спирається закон збереження енергії, не варто нічого не буде зрозуміло. Тому спершу нагадаємо їх читачам.
Термодинаміка розглядає будь-яку річ чи об'єкт як поєднання дуже великої кількості елементарних частин – атомів, іонів, молекул. Її рівняння описують будь-яку зміну колективного стану системи як цілого і частини цілого при зміні макропараметрів. Під останніми розуміються температура (позначається як Т), тиск (Р), концентрація компонентів (зазвичай, З).
Внутрішня енергія
Внутрішня енергія - досить складний термін, у сенсі якого варто розібратися, перш ніж говорити про кількість теплоти. Він позначає ту енергію, яка змінюється зі збільшенням чи зменшенні значення макропараметрів об'єкта і залежить від системи отсчета. Є частиною загальної енергії. Збігається з нею в умовах, коли центр мас досліджуваної речі спочиває (тобто відсутня кінетична складова).
Коли людина відчуває, що деякий об'єкт (скажімо, велосипед) нагрівся або охолонуло, це показує, що всі молекули та атоми, що становлять цю систему, зазнали зміни внутрішньої енергії. Проте незмінність температури значить збереження цього показника.
Робота та теплота

Внутрішня енергія будь-якої термодинамічної системи може перетворитися двома способами:
- за допомогою здійснення над нею роботи;
- при теплообмін з навколишнім середовищем.
Формула цього процесу виглядає так:
dU=Q-А, де U – внутрішня енергія, Q – теплота, А – робота.
Нехай читач не спокушається простотою висловлювання. Перестановка показує, що Q=dU+А, проте введення ентропії (S) наводить формулу виду dQ=dSxT.
Так як в даному випадку рівняння набуває вигляду диференціального, то і перше вираз вимагає того ж. Далі, залежно від сил, що діють в об'єкті, що досліджується, і параметра, який обчислюється, виводиться необхідне співвідношення.
Візьмемо як приклад термодинамічної системи металеву кульку. Якщо на нього натиснути, підкинути вгору, впустити в глибокий колодязь, це означає зробити над ним роботу. Суто зовні всі ці нешкідливі дії кульки ніякої шкоди не завдадуть, але внутрішня енергія її зміниться, хоч і дуже ненабагато.
Другий спосіб – це теплообмін. Тепер підходимо до головної мети цієї статті: опис того, що така кількість теплоти. Це така зміна внутрішньої енергії термодинамічної системи, яка відбувається при теплообміні (див. формулу вище). Воно вимірюється у джоулях чи калоріях. Очевидно, що якщо кульку потримати над запальничкою, на сонці, або просто в теплій руці, то вона нагріється. А далі можна змінити температуру знайти кількість теплоти, яку йому було при цьому повідомлено.
Чому газ – найкращий приклад зміни внутрішньої енергії, і чому через це школярі не люблять фізику

Вище ми описували зміни термодинамічних параметрів металевої кульки. Вони без спеціальних приладів не дуже помітні, і читачеві залишається повірити на слово про процеси, що відбуваються з об'єктом. Інша річ, якщо система – газ. Натисніть на нього – це буде видно, нагрійте – підніметься тиск, опустіть під землю – і це можна легко зафіксувати. Тому в підручниках найчастіше як наочна термодинамічна система беруть саме газ.
Але, на жаль, у сучасній освіті реальним дослідам приділяється не так багато уваги. Вчений, який пише методичний посібник, добре розуміє, про що йдеться. Йому здається, що на прикладі молекул газу всі термодинамічні параметри будуть належним чином продемонстровані. Але учневі, який тільки відкриває собі цей світ, нудно слухати про ідеальну колбу з теоретичним поршнем. Якби в школі існували справжні дослідні лабораторії і на роботу в них виділялися годинники, все було б інакше. Поки що, на жаль, досліди лише на папері. І, швидше за все, саме це стає причиною того, що люди вважають цей розділ фізики чимось суто теоретичним, далеким від життя та непотрібним.

Тому ми вирішили як приклад навести вже згадуваний велосипед. Людина тисне на педалі – здійснює над ними роботу. Крім повідомлення всьому механізму моменту, що крутить (завдяки якому велосипед і переміщається в просторі), змінюється внутрішня енергія матеріалів, з яких зроблені важелі. Велосипедист натискає на ручки, щоб повернути - і знову здійснює роботу.
Внутрішня енергія зовнішнього покриття (пластику чи металу) збільшується. Людина виїжджає на галявину під яскраве сонце – велосипед нагрівається, змінюється його кількість теплоти. Зупиняється відпочити в тіні старого дуба і система охолоджується, втрачаючи калорії або джоулі. Збільшує швидкість – зростає обмін енергією. Однак розрахунок кількості теплоти у всіх цих випадках покаже дуже невелику, непомітну величину. Тому і здається, що проявів термодинамічної фізики у реальному житті немає.
Застосування розрахунків щодо зміни кількості теплоти
Ймовірно, читач скаже, що все це дуже пізнавально, але навіщо нас так мучать у школі цими формулами. А зараз ми наведемо приклади, в яких сферах людської діяльності вони потрібні безпосередньо і як це стосується будь-кого в його повсякденності.
Для початку подивіться навколо себе та порахуйте: скільки предметів із металу вас оточують? Напевно, більше десяти. Але перш ніж стати скріпкою, вагоном, кільцем чи флешкою, будь-який метал проходить виплавку. Кожен комбінат, на якому переробляють, скажімо, залізну руду, повинен розуміти, скільки потрібно палива, щоб оптимізувати витрати. А розраховуючи це, необхідно знати теплоємність металовмісної сировини та кількість теплоти, яку йому необхідно повідомити, щоб відбулися всі технологічні процеси. Оскільки енергія, що виділяється одиницею палива, розраховується в джоулях або калоріях, то формули потрібні безпосередньо.
Або інший приклад: у більшості супермаркетів є відділ із замороженими товарами – рибою, м'ясом, фруктами. Там, де сировина з м'яса тварин чи морепродуктів перетворюється на напівфабрикат, повинні знати, скільки електрики вживуть холодильні та морозильні установки на тонну чи одиницю готового продукту. Для цього слід розрахувати, скільки теплоти втрачає кілограм полуниці або кальмарів при охолодженні на один градус Цельсія. А в результаті це покаже, скільки електрики витратить морозильник певної потужності.
Літаки, пароплави, поїзди

Вище ми показали приклади щодо нерухомих, статичних предметів, яким повідомляють або які, навпаки, забирають певну кількість теплоти. Для об'єктів, що в процесі роботи рухаються в умовах постійної температури, розрахунки кількості теплоти важливі з іншої причини.
Є таке поняття, як "втома металу". Включає воно також і гранично допустимі навантаження при певній швидкості зміни температури. Уявіть, літак злітає із вологих тропіків у заморожені верхні шари атмосфери. Інженерам доводиться багато працювати, щоб він не розвалився через тріщини в металі, які з'являються при перепаді температури. Вони шукають такий склад сплаву, який може витримати реальні навантаження і матиме великий запас міцності. А щоб не шукати наосліп, сподіваючись випадково натрапити на потрібну композицію, доводиться робити багато розрахунків, у тому числі й тих, що включають зміни кількості теплоти.
У цьому уроці ми навчимося розраховувати кількість теплоти, необхідну для нагрівання тіла або виділене ним при охолодженні. Для цього ми узагальнимо ті знання, які були отримані на попередніх уроках.
Крім того, ми навчимося за допомогою формули для кількості теплоти виражати інші величини цієї формули і розраховувати їх, знаючи інші величини. Також буде розглянуто приклад задачі із рішенням на обчислення кількості теплоти.
Даний урок присвячений обчисленню кількості теплоти при нагріванні тіла або виділеного ним при охолодженні.
Вміння обчислювати потрібну кількість теплоти є дуже важливим. Це може знадобитися, наприклад, при обчисленні кількості теплоти, яку потрібно повідомити воді для обігріву приміщення.
Мал. 1. Кількість теплоти, яку необхідно повідомити воді для обігріву приміщення
Або для обчислення кількості теплоти, що виділяється при спалюванні палива у різних двигунах:

Мал. 2. Кількість теплоти, що виділяється при спалюванні палива у двигуні
Також ці знання потрібні, наприклад, щоб визначити кількість теплоти, що виділяється Сонцем та потрапляє на Землю:

Мал. 3. Кількість теплоти, що виділяється Сонцем і потрапляє на Землю
Для обчислення кількості теплоти необхідно знати три речі (рис. 4):
- масу тіла (яку, як правило, можна виміряти за допомогою ваг);
- різницю температур, яку необхідно нагріти тіло чи охолодити його (зазвичай вимірюється з допомогою термометра);
- питому теплоємність тіла (яку можна визначити за таблицею).

Мал. 4. Що потрібно знати для визначення
Формула, за якою обчислюється кількість теплоти, виглядає так:
У цій формулі фігурують такі величини:
Кількість теплоти, що вимірюється в джоулях (Дж);
Питома теплоємність речовини, що вимірюється в ;
- різниця температур, що вимірюється в градусах Цельсія ().
Розглянемо завдання обчислення кількості теплоти.
Завдання
У мідній склянці масою грам знаходиться вода об'ємом літра при температурі. Яку кількість теплоти необхідно передати склянці з водою, щоб її температура дорівнювала ?

Мал. 5. Ілюстрація умови завдання
Спочатку запишемо коротку умову ( Дано) і переведемо всі величини до системи інтернаціонал (СІ).
|
Дано: |
СІ |
|
|
Знайти: |
Рішення:
Спочатку визнач, які ще величини будуть потрібні нам для вирішення цього завдання. За таблицею питомої теплоємності (табл. 1) знаходимо (питома теплоємність міді, оскільки за умовою склянка мідна), (питома теплоємність води, оскільки за умовою у склянці знаходиться вода). Крім того, знаємо, що для обчислення кількості теплоти нам знадобиться маса води. За умовою нам дано лише обсяг. Тому з таблиці візьмемо густину води: (табл. 2).
Табл. 1. Питома теплоємність деяких речовин,
Табл. 2. Щільності деяких рідин
Тепер у нас є все необхідне для вирішення цього завдання.
Зауважимо, що підсумкова кількість теплоти складатиметься із суми кількості теплоти, необхідної для нагрівання мідної склянки та кількості теплоти, необхідної для нагрівання води в ньому:
Розрахуємо спочатку кількість теплоти, необхідну для нагрівання мідної склянки:
Перш ніж обчислити кількість теплоти, необхідну для нагрівання води, розрахуємо масу води за формулою, яка добре знайома нам з 7 класу:
Тепер можемо обчислити:
Тоді можемо обчислити:
Нагадаємо, що означає: кілоджоулі. Приставка «кіло» означає , тобто ![]() .
.
Відповідь:.
Для зручності розв'язання задач на знаходження кількості теплоти (так звані прямі завдання) та пов'язаних з цим поняттям величин можна користуватися наступною таблицею.
|
Шукана величина |
Позначення |
Одиниці виміру |
Основна формула |
Формула для величини |
|
Кількість теплоти |
Процес передачі енергії від одного тіла до іншого без виконання роботи називається теплообміномабо теплопередачею. Теплообмін відбувається між тілами, що мають різну температуру. При встановленні контакту між тілами з різними температурами відбувається передача частини внутрішньої енергії від тіла з вищою температурою тілу, у якого температура нижче. Енергія, передана тілу внаслідок теплообміну, називається кількістю теплоти.
Питома теплоємність речовини:
Якщо процес теплопередачі не супроводжується роботою, то на підставі першого закону термодинаміки кількість теплоти дорівнює зміні внутрішньої енергії тіла: .
Середня енергія безладного поступального руху молекул пропорційна до абсолютної температури. Зміна внутрішньої енергії тіла дорівнює сумі алгебри змін енергії всіх атомів або молекул, число яких пропорційно масі тіла, тому зміна внутрішньої енергії і, отже, кількість теплоти пропорційно масі і зміні температури:


Коефіцієнт пропорційності у цьому рівнянні називається питомою теплоємністю речовини. Питома теплоємність показує, скільки теплоти необхідне нагрівання 1 кг речовини на 1 До.
Робота в термодинаміці:
У механіці робота визначається як добуток модулів сили та переміщення та косинуса кута між ними. Робота відбувається при дії сили на тіло, що рухається, і дорівнює зміні його кінетичної енергії.
У термодинаміці рух тіла як цілого не розглядається, йдеться про переміщення частин макроскопічного тіла щодо один одного. У результаті змінюється об'єм тіла, яке швидкість залишається рівної нулю. Робота в термодинаміці визначається так само, як і в механіці, але дорівнює зміні кінетичної енергії тіла, а його внутрішньої енергії.
При виконанні роботи (стисненні чи розширенні) змінюється внутрішня енергія газу. Причина цього полягає в наступному: при пружних зіткненнях молекул газу з поршнем, що рухається, змінюється їх кінетична енергія.
Обчислимо роботу газу під час розширення. Газ діє на поршень із силою  , де
, де  - тиск газу, а
- тиск газу, а  - площа поверхні
- площа поверхні  поршня. При розширенні газу поршень зміщується у напрямку сили
поршня. При розширенні газу поршень зміщується у напрямку сили  на малу відстань
на малу відстань  . Якщо відстань мала, то тиск газу вважатимуться постійним. Робота газу дорівнює:
. Якщо відстань мала, то тиск газу вважатимуться постійним. Робота газу дорівнює:
Де  - Зміна обсягу газу.
- Зміна обсягу газу.
У процесі розширення газу здійснює позитивну роботу, оскільки напрям сили та переміщення збігаються. У процесі розширення газ віддає енергію оточуючим тілам.
Робота, що здійснюється зовнішніми тілами над газом, відрізняється від роботи газу тільки знаком  , оскільки сила
, оскільки сила  , що діє на газ, протилежна силі
, що діє на газ, протилежна силі  , з якою газ діє поршень, і дорівнює їй по модулю (третій закон Ньютона); а переміщення залишається тим самим. Тому робота зовнішніх сил дорівнює:
, з якою газ діє поршень, і дорівнює їй по модулю (третій закон Ньютона); а переміщення залишається тим самим. Тому робота зовнішніх сил дорівнює:
 .
.
Перший закон термодинаміки:
Перший закон термодинаміки є законом збереження енергії, поширеним на теплові явища. Закон збереження енергії: енергія в природі не виникає з нічого і не зникає: кількість енергії незмінна, вона лише переходить із однієї форми до іншої.
У термодинаміці розглядаються тіла, становище центру тяжкості яких мало змінюється. Механічна енергія таких тіл залишається постійною, а може змінюватися лише внутрішня енергія.
Внутрішня енергія може змінюватися двома способами: теплопередачею та виконанням роботи. У випадку внутрішня енергія змінюється як з допомогою теплопередачі, і з допомогою робіт. Перший закон термодинаміки формулюється саме для таких загальних випадків:
Зміна внутрішньої енергії системи при переході її з одного стану в інший дорівнює сумі роботи зовнішніх сил та кількості теплоти, переданої системі:

Якщо система ізольована, то над нею не відбувається робота і вона не обмінюється теплотою з оточуючими тілами. Відповідно до першого закону термодинаміки внутрішня енергія ізольованої системи залишається незмінною.
Враховуючи що  , Перший закон термодинаміки можна записати так:
, Перший закон термодинаміки можна записати так:

Кількість теплоти, передане системі, йде зміну її внутрішньої енергії і здійснення системою роботи над зовнішніми тілами.
Другий закон термодинаміки: неможливо перевести теплоту від холоднішої до гарячішої за відсутності інших одночасних змін в обох системах або в навколишніх тілах.
(або теплопередачі).
Питома теплоємність речовини.
Теплоємність- Це кількість теплоти, що поглинається тілом при нагріванні на 1 градус.
Теплоємність тіла позначається великою латинською літерою З.
Від чого залежить теплоємність тіла? Насамперед, від його маси . Ясно, що для нагрівання, наприклад, 1 кілограма води потрібно більше тепла, ніж для нагрівання 200 грамів.
А від роду речовини? Зробимо досвід. Візьмемо дві однакові судини і, наливши в одну з них воду масою 400 г, а в іншій — олію масою 400 г, почнемо їх нагрівати за допомогою однакових пальників. Спостерігаючи за показаннями термометрів, ми побачимо, що олія нагрівається швидке. Щоб нагріти воду та олію до однієї і тієї ж температури, воду слід нагрівати довше. Але чим довше ми нагріваємо воду, тим більше теплоти вона отримує від пальника.
Таким чином, для нагрівання однієї і тієї ж маси різних речовин до однакової температури потрібна різна кількість теплоти. Кількість теплоти, необхідне нагрівання тіла і, отже, його теплоємність залежить від роду речовини, з якого складається це тіло.
Так, наприклад, щоб збільшити на 1 ° С температуру води масою 1 кг, потрібна кількість теплоти, що дорівнює 4200 Дж, а для нагрівання на 1 ° С такої ж маси соняшникової олії необхідна кількість теплоти, що дорівнює 1700 Дж.
Фізична величина, що показує, скільки теплоти потрібно для нагрівання 1 кг речовини на 1 ºС, називається питомою теплоємністюцієї речовини.
У кожної речовини своя питома теплоємність, яка позначається латинською літерою с і вимірюється в джоулях на кілограм-градус (Дж/(кг · ° С)).
Питома теплоємність однієї й тієї ж речовини в різних агрегатних станах (твердому, рідкому та газоподібному) різна. Наприклад, питома теплоємність води дорівнює 4200 Дж/(кг · ºС), а питома теплоємність льоду 2100 Дж/(кг · °С); алюміній у твердому стані має питому теплоємність, що дорівнює 920 Дж/(кг - °С), а в рідкому - 1080 Дж/(кг - °С).
Зауважимо, що вода має дуже велику питому теплоємність. Тому вода в морях та океанах, нагріваючись улітку, поглинає з повітря велику кількість тепла. Завдяки цьому в тих місцях, які розташовані поблизу великих водойм, літо не буває таким спекотним, як у місцях віддалених від води.
Розрахунок кількості теплоти, необхідної для нагрівання тіла або виділеного ним при охолодженні.
З вищевикладеного ясно, що кількість теплоти, необхідне нагрівання тіла, залежить від роду речовини, з якого складається тіло (тобто його питомої теплоємності), і зажадав від маси тіла. Зрозуміло також, що кількість теплоти залежить від того, скільки градусів ми збираємося збільшити температуру тіла.
Отже, щоб визначити кількість теплоти, необхідну для нагрівання тіла або виділене ним при охолодженні, потрібно питому теплоємність тіла помножити на його масу і на різницю між кінцевою і початковою температурами:
Q = cm (t 2 - t 1 ) ,
де Q- кількість теплоти, c- питома теплоємність, m- маса тіла , t 1 - Початкова температура, t 2 - Кінцева температура.
При нагріванні тіла t 2 > t 1 і, отже, Q > 0 . При охолодженні тіла t 2і< t 1 і, отже, Q< 0 .
Якщо відома теплоємність всього тіла З, Qвизначається за формулою:
Q = C (t 2 - t 1 ) .