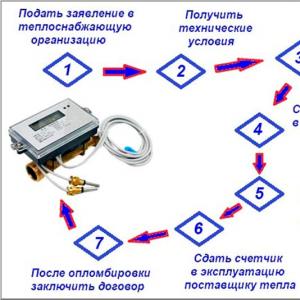
Фізико-хімічні методи пом'якшення води. Шкідливість жорсткої води та способи її пом'якшення У яких установках відбувається пом'якшення води
Вода має винятково високу розчинну здатність. Випадаючи у вигляді атмосферних опадів, вона розчиняє гази, що знаходяться в атмосфері, в тому числі і вуглекислий газ. Надалі просочуючись у землю, вода захоплює додаткова кількістьвуглекислого газу як продукту розкладання об'єктів живої та не живої природи. Взаємодіючи з водою вуглекислий газ утворює вугільну кислоту, збільшуючи потенціал для розчинення мінералів та інших домішок. Проходячи через шар вапняку, вона насичується іонами кальцію та магнію, відповідальними за жорсткість. Залізо і марганець у джерелах перебувають у менших концентраціях, ніж іони кальцію та магнію. Оскільки вода є розчинником, вона захоплює розчинні хлориди, сульфати, нітрати кальцію та магнію. Схожим чином вона поглинає карбонатні, бікарбонатні, хлоридні, сульфатні сполуки натрію, а також деяку кількість кремнезему.
У загальному випадку, при докладному аналізіу ній можуть бути виявлені у більшій чи меншій концентрації практично всі елементи таблиці Менделєва.
Жорсткістьпідрозділяється на гідрокарбонатну, звану ще тимчасову, і некарбонатну (хлоридну, сульфатну, нітратну) - постійну. Тимчасова жорсткістьусувається при кип'ятінні (наліт на нагрівальному елементі), постійна жорсткістьпри нагріванні не усувається.
Очищення від солей жорсткості називається пом'якшенням. Жорсткість води біля РФ вимірюється в одиницях мг-экв/литр і, залежно від галузі використання, вимоги до рівня жорсткості змінюються від 7 мг-экв/л (господарсько-побутові цілі) до одиниць мг-экв/литр і менше у медицині , електроніки, енергетики, атомної промисловості. Допустима жорсткість води 7 мг-екв/л не несе серйозної небезпеки здоров'ю, але створює цілий ряд побутових проблем. Жорстка вода викликає утворення опадів та нальотів на поверхні трубопроводів та робочих елементах побутової техніки. Ця проблема особливо актуальна для приладів з нагрівальними елементами – водогрійних та парових котлів, бойлерів та іншого теплообмінного обладнання.
Усунення жорсткості – пом'якшення здійснюється за допомогою іоннообмінної смоли. Іоннообмінна смола являє собою полімер, що складається з полімерної матриці та функціональних груп. Полімерна матриця синтезується з мономеру стиролу в присутності дивінілбензолу, що зв'язує. У процесі синтезу використовується спирт, який у певний момент випаровується, і, виходячи з матриці, формує в ній пори. Потім матрицю вводяться функціональні групи. Функціональна група складається з двох частин: нерухомої, прикріпленої до матриці, та рухомої частини. Якщо рухомою частиною функціональної групи служить катіон, а нерухомий - аніон, то смола називається катіонообмінною, а якщо рухлива частина аніон - аніонообмінною. Катіонообмінна смола може бути в натрієвій формі (Na-катіонообмінна смола) або у водневій формі (H-катіонообмінна смола).
Процес пом'якшення іоннообмінної смолою
Очищення іонообмінними смолами
Іонообмінна смола засипається в колону, заповнюючи 60-65% загального обсягу фільтра. Жорстка вода надходить у колону і, оскільки іонообмінний матеріал має більшу хімічну спорідненість із кальцієм і магнієм, ніж з іонами натрію, останні витісняються ними зі смоли. Заміна катіонів кальцію та магнію на катіони натрію відбувається в еквівалентних співвідношеннях. Вода, що містить на вході іони бікарбонату кальцію та магнію, на виході з нього міститиме еквівалентну кількість бікарбонатів натрію. Кількість іонів натрію на смолі обмежена, тому настає момент, коли смола перестає пом'якшувати воду, тобто вичерпано обмінну ємність смоли. Для перезарядки смоли або її регенерації запускається процес зворотного іонного обміну, в ході якого іонообмінна смола піддається вплив концентрованим розчином вихідного виду катіонів. Для регенерації Na-катіонообмінної смоли використовують відносно міцний розчинхлориду натрію. Натрій із розчину витісняє кальцій та магній зі смоли, перезаряджаючи її.
Установка пом'якшення, очищення іонообмінними смолами:
Конструктивно встановлення пом'якшення складається з трьох частин: балони з іонообмінною смолою та водопідйомною трубкою, клапана управління з електронним контролером та ємності для сольового розчину. Контролери бувають двох видів: регенерація відбувається за часом та регенерація відбувається за обсягом. При регенерації за часом контролер переводить установку режим регенерації через певну кількість годин, днів чи певний день тижня. При регенерації за обсягом клапан управління має вбудований лічильник води і через певну кількість води, що пройшла через установку води, контролер переводить її в режим регенерації. Цей обсяг називається фільтроциклом установки та розраховується контролером на основі жорсткості води, об'єму та ємності завантаження, які вводяться в контролер на стадії програмування.
У тих випадках, коли потрібне безперебійне забезпечення м'якою водою, можуть застосовуватись два однакові фільтри, що функціонують у режимі TWIN або DUPLEX. У режимі «твін» один контролер керує двома клапанами керування. Коли один фільтр пом'якшує воду, знаходиться в робочому режимі, другий з відрегенерованою смолою знаходиться в режимі очікування. Коли фільтроцикл першого фільтра вичерпано, клапан управління переводить другий фільтр у робочий режим фільтрації, а перший - режим регенерації. Після завершення регенерації перший фільтр переходить в режим очікування, і знаходиться в ньому, доки не закінчиться фільтроцикл другого. Процес очищення циклічно повторюється, фільтри працюють поперемінно.
У режимі «дуплекс» фільтри функціонують одночасно і по черзі переводяться за заданою програмою режим регенерації зі зрушенням за часом її початку тривалість циклу регенерації.
Пом'якшення води вапнуванням
У тих випадках, коли необхідно пом'якшувати воду з високою карбонатною жорсткістю (понад 30 мг-екв/л) недоцільно застосовувати іонообмінну смолу. Попередньо слід знизити жорсткість, використовуючи технологію вапнування. Пом'якшення води вапном і кальцинованою содою передбачає дозування гашеного вапна Сa(OH)2 у жорстку воду для видалення карбонатної жорсткості шляхом осадження та подальшого фільтрування осаду. Некарбонатна жорсткість у свою чергу зменшується додаванням кальцинованої соди Na2CO3 для формування нерозчинного осаду, який також видаляється фільтруванням.
Даний метод використовується на водоканалах та підприємствах з великим споживанням води. Це досить ефективний методЗменшення жорсткості води, однак, він не дозволяє повністю видалити всі мінерали.
Гашене вапно застосовується для видалення бікарбонату кальцію з води. Там, де кальцій та магній містяться у формі хлоридів або сульфатів, така обробка помітно менш ефективна.
Зменшення жорсткості води вапном та кальцинованою содою стає надзвичайно дорогим, якщо жорсткість треба знизити до рівня менше 2 мг-екв/л. Для побутових цілей пом'якшення води вапном та кальцинованою содою є непрактичним. З одного боку - є труднощі в подачі вапна та кальцинованої соди, з іншого боку - потрібен суворий контроль процесу відстоювання та фільтрації. Ще одним стримуючим фактором використання цього процесу є розміри необхідного обладнанняі велика кількість вапняного шламу, що викидається.
Пом'якшення води діалізом
Магнітна обробка води
Література
Теоретичні основи пом'якшення води, класифікація методів
Під пом'якшенням води мається на увазі процес видалення із неї катіонів жорсткості, тобто. кальцію та магнію.Відповідно до ГОСТ 2874-82 "Вода питна" жорсткість води не повинна перевищувати 7 мг-екв/л. Окремі видивиробництв до технологічної води висувають вимоги глибокого її пом'якшення, тобто. до 0,05.0,01 мг-екв/л. Зазвичай використовувані вододжерела мають жорсткість, що відповідає нормам господарсько-питних вод, і пом'якшення не потребують. Пом'якшення води виробляють в основному під час її підготовки для технічних цілей. Так, жорсткість води для живлення барабанних котлів має перевищувати 0,005 мг-экв/л. Пом'якшення води здійснюють методами: термічним, заснованим на нагріванні води, її дистиляції або виморожуванні; реагентними, при яких іони, що знаходяться у воді Ca ( II ) та Mg ( II ) пов'язують різними реагентами практично нерозчинні сполуки; іонного обміну, заснованого на фільтруванні пом'якшувальної води через спеціальні матеріали, що обмінюють іони, що входять до їх складу. Na ( I) або Н (1) на іони Са (II) та Mg ( II ), що містяться у воді діалізу; комбінованим, що є різними поєднаннями перерахованих методів.
Вибір методу пом'якшення води визначається її якістю, необхідною глибиною пом'якшення та техніко-економічними міркуваннями. Відповідно до рекомендацій СНіПу при пом'якшенні підземних водслід застосовувати іонообмінні методи; при пом'якшенні поверхневих вод, коли одночасно потрібне і освітлення води, - вапняний або вапняно-содовий метод, а при глибокому пом'якшенні води - подальше катіонування.Основні характеристики та умови застосування методів пом'якшення води наведено у табл. 20.1.
пом'якшення вода діаліз термічний
Для отримання води для господарсько-питних потреб зазвичай пом'якшують лише її деяку частину з наступним змішуванням з вихідною водою, при цьому кількість води, що пом'якшується. Q yвизначають за формулою
де Ж о. в. - загальна жорсткість вихідної води, мг-екв/л; Ж 0. с. - загальна жорсткість води, що надходить до мережі, мг-екв/л; Ж 0.у. - Жорсткість пом'якшеної води, мг-екв/л.
Методи пом'якшення води
| Показник | термічний | реагентний | іонообмінний | діалізу |
| Характеристика процесу | Воду нагрівають до температури вище 100°С, при цьому видаляється карбонатна і некарбонатна жорсткості (у вигляді карбонату кальцію, гідрокси- та магнію і гіпсу). | У воду додають вапно, що усуває карбонатну і магнієву жорсткість, а також соду, що усуває некарбонат - іншу жорсткість | Пом'якшувальна вода пропускається через катіонітові фільтри | Вихідна вода фільтрується через напівпроникну мембрану |
| Призначення методу | Усунення карбонатної жорсткості з води, що використовується для живлення котлів низького н середнього тиску | Неглибоке пом'якшення при одночасному освітленні води від завислих речовин | Глибоке пом'якшення води, що містить незначну кількість завислих речовин | Глибоке пом'якшення води |
| Витрата води на власні потреби | - | Не більше 10% | До 30% і більше пропорційно жорсткості вихідної води | 10 |
| Умови ефективного застосування: каламутність вихідної води, мг/л | До 50 | До 500 | Не більше 8 | До 2,0 |
| Жорсткість води, мг-екв/л | Карбонатна жорсткість з переважанням Са (НС03) 2, некарбонатна жорсткість у вигляді гіпсу | 5.30 | Не вище 15 | До 10,0 |
| Залишкова жорсткість води, мг-екв/л | Карбонатна жорсткість до 0,035, CaS04 до 0,70 | До 0,70 | 0,03.0,05 прн одноступінчастому і до 0,01 при двоступінчастому катіонуванні | 0,01 і нижче |
| Температура води, ° С | До 270 | До 90 | До 30 (глауконіт), до 60 (сульфовугілля) | До 60 |
Термічний метод пом'якшення води
Термічний метод пом'якшення води доцільно застосовувати під час використання карбонатних вод, що йдуть харчування котлів низького тиску, і навіть у поєднанні з реагентними методами пом'якшення води. Він заснований на усуненні вуглекислотної рівноваги при її нагріванні у бік утворення карбонату кальцію, що описується реакцією
Са (НС0 3) 2 -> СаСО 3 + С0 2 + Н 20.
Рівнавага зміщується за рахунок зниження розчинності оксиду вуглецю (IV), що викликається підвищенням температури та тиску. Кип'ятінням можна повністю видалити оксид вуглецю (IV) і цим значно знизити карбонатну кальцієву жорсткість. Однак, повністю усунути зазначену жорсткість не вдається, оскільки карбонат кальцію хоча і незначно (13 мг/л при температурі 18°С), але все ж таки розчинний у воді.
За наявності у воді гідрокарбонату магнію процес його осадження відбувається так: спочатку утворюється порівняно добре розчинний (110 мг/л при температурі 18° С) карбонат магнію
Mg (НСО 3) → MgC0 3 + С0 2 + Н 2 0,
який при тривалому кип'ятінні гідролізується, внаслідок чого випадає осад малорозчинного (8,4 мг/л). гідроксиду магнію
MgC0 3 +H 2 0 → Mg (0H) 2 +C0 2 .
Отже, при кип'ятінні води жорсткість, що обумовлюється гідрокарбонатами кальцію та магнію, знижується. При кип'ятінні води знижується також жорсткість, яка визначається сульфатом кальцію, розчинність якого падає до 0,65 г/л.
На рис. 1 показаний термопом'якшувач конструкції Коп'єва, що відрізняється відносною простотою пристрою та надійністю роботи. Попередньо підігріта в апараті вода, що обробляється, надходить через ежектор на розетку плівкового підігрівача і розбризкується над вертикально розміщеними трубами, і по них стікає вниз назустріч гарячій парі. Потім разом з продувною водою від котлів вона по трубі, що центрально подає, через дірчасте днище надходить у освітлювач зі зваженим осадом.
Вуглекислота, що виділяється при цьому з води, і кисень разом з надлишком пари скидаються в атмосферу. Солі кальцію і магнію, що утворюються в процесі нагрівання води, затримуються у зваженому шарі. Пройшовши через зважений шар, пом'якшена вода надходить до збірки та відводиться за межі апарату.
Час перебування води в термопом'якшувачі становить 30.45 хв, швидкість її висхідного руху у завислому шарі 7.10 м/год, а в отворах хибного дна 0,1.0,25 м/с.

Рис. 1. Термопом'якшувач конструкції Коп'єва.
15 - скидання дренажної води; 12 - центральна труба, що подає; 13 - хибні перфоровані днища; 11 - зважений шар; 14 - скидання шламу; 9 - збірка пом'якшеної води; 1, 10 2 - продування котлів; 3 - ежектор; 4 - Випар; 5 - плівковий підігрівач; 6 - скидання пари; 7 - кільцевий перфорований трубопровід відведення води до ежектора; 8 - похилі перегородки, що сепарують.
Реагентні методи пом'якшення води
Пом'якшення води реагентними методами засноване на обробці її реагентами, що утворюють з кальцієм і магнієм малорозчинні сполуки: Mg (OH) 2 , СаС0 3 Са 3 (Р0 4) 2 , Mg 3 (P0 4) 2 та інші з подальшим їх відділенням в освітлювачах , тонкошарових відстійниках та освітлювальних фільтрах. Як реагентів використовують вапно, кальциновану соду, гідроксиди натрію та барію та інші речовини.
Пом'якшення води вапнуваннямзастосовують при її високій карбонатній та низькій некарботаній жорсткості, а також у разі, коли не потрібно видаляти з води солі некарбонатної жорсткості. Як реагент використовують вапно, яке вводять у вигляді розчину або суспензії (молоку) попередньо підігріту оброблювану воду. Розчиняючись, вапно збагачує воду іонами ОН - і Са 2+ , що призводить до зв'язування розчиненого у воді вільного оксиду вуглецю (IV) з утворенням карбонатних іонів та переходу гідрокарбонатних іонів у карбонатні:
С0 2 + 20Н - → ЗІ 3 + Н 2 0, НСО 3 - + ВІН - → ЗІ 3 - + Н 2 О.
Підвищення в оброблюваній воді концентрації іонів С0 3 2 - і присутність у ній іонів Са 2+ з урахуванням введених з вапном призводить до підвищення твору розчинності та осадження малорозчинного карбонату кальцію:
Са 2+ С0 3 - → СаС0 3 .
При надлишку вапна в осад випадає і гідроксид магнію
Mg 2+ + 20Н - → Mg (ОН) 2
Для прискорення видалення дисперсних та колоїдних домішок та зниження лужності води одночасно з вапнуванням застосовують коагуляцію цих домішок сульфатом заліза (II), тобто. FeS0 4 *7 Н 2 0. Залишкова жорсткість пом'якшеної води при декарбонізації може бути отримана на 0,4.0,8 мг-екв/л більше некарбонатної жорсткості, а лужність 0,8.1,2 мг-екв/л. Доза вапна визначається співвідношенням концентрації у воді іонів кальцію та карбонатної жорсткості: а) при співвідношенні [Са 2+] /20<Ж к,
б) при співвідношенні [Са 2+] /20 > Ж к,
де [СО 2 ] - Концентрація у воді вільного оксиду вуглецю (IV), мг/л; [Са 2+] - концентрація іонів кальцію, мг/л; Ж к - карбонатна жорсткість води, мг-екв/л; Д до - доза коагулянту (FeS0 4 або FeCl 3 у перерахунку на безводні продукти), мг/л; е до- еквівалентна маса активної речовини коагулянту, мг/мг-екв (для FeS0 4 едо = 76, для FeCl 3 е к = 54); 0,5 і 0,3 - надлишок вапна для забезпечення більшої повноти реакції, мг-екв/л.
Вираз Д к / е к беруть зі знаком мінус, якщо коагулянт вводиться раніше вапна, і зі знаком плюс, якщо спільно або після.
За відсутності експериментальних даних дозу коагулянту знаходять із виразу
Д до = 3 (С) 1/3 , (20.4)
де С - кількість суспензії, що утворюється при пом'якшенні води (у перерахунку на суху речовину), мг/л.
У свою чергу, С визначають, використовуючи залежність
де М і - вміст завислих речовин у вихідній воді, мг/л; m- Зміст СаО в товарній вапні, %.
Вапняно-содовий метод пом'якшення водиописується наступними основними реакціями:

За цим методом залишкова жорсткість може бути доведена до 0,5.1 а лужність з 7 до 0,8.1,2 мг-екв/л.
Дози вапна Д та та соди Д с (у перерахунку на Na 2 C0 3), мг/л, визначають за формулами
![]() (20.7)
(20.7)
де - вміст у воді магнію, мг/л; Ж н. к. – некарбонатна жорсткість води, мг-екв/л.
При вапняно-содовому методі пом'якшення води, що утворюються, карбонат кальцію і гідроксид магнію можуть пересичувати розчини і довго залишатися в колоїдно-дисперсному стані. Їх перехід у грубодисперсний шлам тривалий, особливо при низьких температурах та наявності у воді органічних домішок, які діють як захисні колоїди. При велику їх кількість жорсткість води при реагентному пом'якшенні води може знижуватися всього на 15.20%. У подібних випадках перед пом'якшенням або в процесі його видаляють з води органічні домішки окислювачами і коагулянтами. При вапняно-содовому методі часто проводять у дві стадії. Спочатку з води видаляють органічні домішки та значну частину карбонатної жорсткості,використовуючи солі алюмінію або заліза з вапном, проводячи процес за оптимальних умов коагуляції. Після цього вводять соду і решту вапна і пом'якшують воду.При видаленні органічних домішок одночасно з пом'якшенням води як коагулянти застосовують тільки солі заліза, оскільки при високому значенні рН води, необхідному для видалення магнієвої жорсткості, солі алюмінію не утворюють сорбційно-активного гідроксиду. Дозу коагулянту за відсутності експериментальних даних розраховують за формулою (20.4). Кількість суспензії визначають за формулою
де Ж про - загальна жорсткість води, мг-екв/л.
Більш глибоке пом'якшення води може бути досягнуто її підігрівом, додаванням надлишку реагенту-осадника і створенням контакту води, що пом'якшується, з раніше утвореними опадами. При підігріві води зменшується розчинність СаСО 3 і Mg (OH) 2 і повніше протікають реакції пом'якшення.
З графіка (рис. 2 а) видно, що залишкова жорсткість, близька до теоретично можливої, може бути отримана тільки при значному підігріві води. Значний ефект пом'якшення спостерігається при 35.40 ° С, подальший підігрів менш ефективний. Глибоке пом'якшення ведуть при температурі вище 100° С. Великий надлишок реагенту-осадника при декарбонізації додавати не рекомендується, так як зростає залишкова жорсткість через неперереагував вапна або за наявності у воді магнієвої некарбонатної жорсткості внаслідок її переходу в кальцієву жорсткість:
MgS0 4 + Са (ОН) 2 = Mg (ОН) 2 + CaS0 4

Рис. 2. Вплив температури (а) та дози вапна (б) на глибину пом'якшення води вапняно-содовим та вапняним методом
Са (0H) 2 + Na 2 C0 3 = CaC0 3 +2NaOH,
Проте надлишок вапна призводить до нераціонального перевитрати соди, підвищення вартості пом'якшення води та збільшення гідратної лужності. Тому надлишок соди приймають близько 1 мг-екв/л. Жорсткість води в результаті контакту з осадом, що раніше випав, знижується на 0,3.0,5 мг-екв/л в порівнянні з процесом без контакту з осадком.
Контроль процесу пом'якшення води слід здійснювати корекцією рН пом'якшеної води. Коли це неможливо, його контролюють значення гідратної лужності, яку при декарбонізації підтримують в межах 0,1.0,2 мг-екв/л, при вапняно-содовому пом'якшенні - 0,3.0,5 мг-екв/л.
При содово-натрієвому методі пом'якшення води її обробляють содою та гідроксидом натрію:

Зважаючи на те, що сода утворюється при реакції гідроксиду натрію з гідрокарбонатом, необхідна для добавки у воду доза її значно зменшується. При високій концентрації гідрокарбонатів у воді та низької некарбонатної жорсткості надлишок соди може залишатися в пом'якшеній воді. Тому цей метод застосовують лише з урахуванням співвідношення між карбонатною та некарбонатною жорсткістю.
Содово-натрієвий методзазвичай застосовують для пом'якшення води, карбонатна жорсткість якої трохи більша за некарбонатну. Якщо карбонатна жорсткість приблизно дорівнює некарбонатної, соду можна зовсім не додавати, оскільки необхідну кількість для пом'якшення такої води утворюється в результаті взаємодії гідрокарбонатів з їдким натром. Доза кальцинованої соди збільшується з підвищенням некарбонатної жорсткості води.
Содорегенеративний метод, заснований на відновленні соди в процесі пом'якшення, застосовують при підготовці води для живлення парових котлів низького тиску
Са (НС0 3) 2 + Na 2 C0 3 = СаС0 3 + 2NaHC0 3 .
Гідрокарбонат натрію, потрапляючи в котел із пом'якшеною водою, розкладається під впливом високої температури
2NаHC0 3 = Na 2 C0 3 + Н 2 0 + С0 2 .
Сода, що утворюється при цьому разом з надлишковою, введеною спочатку у водопом'якшувач, тут же в котлі гідролізує з утворенням гідроксиду натрію і оксиду вуглецю (IV), який з продувною водою надходить у водопом'якшувач, де використовується для видалення з пом'якшувальної води гідрокарбонатів кальцію і магнію. Недолік цього методу полягає в тому, що утворення значної кількості 2 в процесі пом'якшення викликає корозію металу і підвищення сухого залишку в котловій воді.
Барієвий метод пом'якшення водизастосовують у поєднанні з іншими методами. Спочатку вводять барій містять реагенти у воду (ВІН) 2 , СО 3 , АА 2 0 4) для усунення сульфатної жорсткості, потім після освітлення води її обробляють вапном і содою для пом'якшення. Хімізм процесу описується реакціями:

Через високу вартість реагентів барієвий метод застосовують дуже рідко. Для підготовки питної води через токсичність барієвих реагентів він непридатний. Сульфат барію, що утворюється, осаджується дуже повільно, тому необхідні відстійники або освітлювачі. великих розмірів. Для введення ВаС03 слід використовувати флокулятори з механічними мішалками, оскільки ВаСО 3 утворює важку суспензію, що швидко осаджується.
Необхідні дози барієвих солей, мг/л, можна знайти, користуючись виразами: гідроксиду барію (продукт 100%-ної активності) Д б =1,8 (SO 4 2-), алюмінату барію Д б =128Ж 0; вуглекислого барію Д = 2,07γ (S0 4 2-);
Вуглекислий барій застосовують із вапном. Шляхом впливу вуглекислоти на карбонат барію отримують бікарбонат барію, який і дозують в воду, що пом'якшується. При цьому дозу вуглекислоти, мг/л визначають з виразу: Д уг. = 0,46 (SO 4 2-); де (S0 4 2-) - вміст сульфатів в пом'якшувальній воді, мг/л; γ=1,15.1,20 - коефіцієнт, що враховує втрати вуглекислого барію.
Оксалатний метод пом'якшення водизаснований на застосуванні оксалату натрію і на малій розчинності у воді оксалату кальцію, що утворюється (6,8 мг/л при 18° С)
Метод відрізняється простотою технологічного та апаратурного оформлення, однак через високу вартість реагенту його застосовують для пом'якшення невеликих кількостей води.
Фосфатування застосовують для пом'якшення води.Після реагентного пом'якшення вапняно-содовим методом неминуче наявність залишкової жорсткості (близько 2 мг-екв/л), яку фосфатним пом'якшенням можна знизити до 0,02-0,03 мг-екв/л. Така глибока доочищення дозволяє в деяких випадках не вдаватися до катіонітового водозм'якшення.
Фосфатуванням досягається також більша стабільність води, зниження її корозійної дії на металеві трубопроводита попереджаються відкладення карбонатів на внутрішній поверхні стінок труб.
Як фосфатних реагентів використовують гексаметафос - фат, триполіфосфат (ортофосфат) натрію та ін.
Фосфатний метод пом'якшення води при використанні три-натрійфосфату є найбільш ефективним реагентним методом. Хімізм процесу пом'якшення води тринатрійфосфатом описується реакціями
Як видно з наведених реакцій, сутність методу полягає в утворенні кальцієвих і магнієвих солей фосфорної кислоти, які мають малу розчинність у воді і тому досить повно випадають в осад.
Фосфатне пом'якшення зазвичай здійснюють при підігріві води до 105.150°, досягаючи її пом'якшення до 0,02.0,03 мг-екв/л. Через високу вартість тринатрійфосфату фосфатний метод зазвичай використовується для пом'якшення води, попередньо пом'якшеним вапном і содою. Доза безводного тринатрійфосфату (Д ф; мг/л) для пом'якшення може бути визначена з виразу
Д Ф =54,67 (Ж ОСТ + 0,18),
де Ж ост - залишкова жорсткість пом'якшеної води перед фосфатним пом'якшенням, мг-екв/л.
Осади Са 3 (Р0 4) 2 і Mg 3 (P0 4) 2, що утворюються при фосфатному пом'якшенні, добре адсорбують з пом'якшеної води органічні колоїди і кремнієву кислоту, що дозволяє виявити доцільність застосування цього методу для підготовки поживної води для котлів середнього і високого тиску (58 , 8.98,0 МПа).
Розчин для дозування гексаметафосфату або ортофосфату натрію з концентрацією 0,5-3% готують у баках, кількість яких має бути не менше двох. Внутрішні поверхністінок і дна баків повинні бути покриті стійким корозійно матеріалом. Час приготування 3%-ного розчину становить 3 години при обов'язковому перемішуванні мішалковим або барботажним (за допомогою стисненого повітря) способом.
Технологічні схеми та конструктивні елементиустановок реагентного пом'якшення води
У технології реагентного пом'якшення води використовують апаратуру для приготування та дозування реагентів, змішувачі, тонкошарові відстійники або освітлювачі, фільтри та установки для стабілізаційної обробки води. Схема напірної водозм'якшувальної установки представлена на рис. 3

Рис. 3. Водопом'якшувальне встановлення з вихровим реактором.
1 - бункер із контактною масою; 2 - ежектор; 3, 8 - подача вихідної та відведення пом'якшеної води; 4 - вихровий реактор; 5 - Введення реагентів; 6 - швидкий освітлювальний фільтр; 9 - скидання контактної маси; 7 - резервуар пом'якшеної води
У цій установці відсутня камера пластів'я, оскільки пластівці осаду карбонату кальцію формуються в контактній масі. При необхідності воду перед реакторами освітлюють.
Оптимальною спорудою для пом'якшення води вапняним чи вапняно-содовим методами є вихровий реактор (спірактор напірний або відкритий) (Рис. 20.4). Реактор є залізобетонним або сталевим корпусом, звуженим донизу (кут конусності 5.20°) і наповнений приблизно до половини висоти контактною масою. Швидкість руху води у нижній вузькій частині вихрового реактора дорівнює 0,8.1 м/с; швидкість висхідного потоку у верхній частині на рівні водовідвідних пристроїв – 4.6 мм/с. Як контактну масу застосовують пісок або мармурову крихту з розміром зерен 0,2.0,3 мм з розрахунку 10 кг на 1 м3 об'єму реактора. При гвинтовому висхідному потоці води контактна маса зважується, піщинки стикаються один з одним і на їх поверхні інтенсивно кристалізується СаСО 3; поступово піщинки перетворюються на кульки правильної форми. Гідравлічний опір контактної маси становить 0,3 м-коду на 1 м висоти. Коли діаметр кульок збільшується до 1,5.2 мм, найбільшу найбільш важку контактну масу випускають з нижньої частини реактора і довантажують свіжу. Вихрові реактори не затримують осаду гідроксиду магнію, тому їх слід застосовувати спільно з встановленими за ними фільтрами тільки в тих випадках, коли кількість осаду гідроксиду магнію, що утворюється, відповідає брудоємності фільтрів.
При брудоємності піщаних фільтрів, що дорівнює 1.1,5 кг/м 3 і фільтроциклі 8 год допустима кількість гідроксиду магнію становить 25.35 г/м 3 (вміст магнію у вихідній воді не повинен перевищувати 10.15 г/м 3). Можливе застосування вихрових реакторів і при більшому вмісті магнію гідроксиду, але при цьому після них необхідно встановлювати освітлювачі для виділення гідроксиду магнію.
Витрата свіжої контактної маси, що додається за допомогою ежектора, визначають за формулою G = 0,045QЖ, де G- кількість контактної маси, що додається, кг/добу; Ж- жорсткість води, що видаляється в реакторі, мг-екв/л; Q – продуктивність установки, м 3 /год.

Рис. 4. Вихровий реактор.
1,8 - подача вихідної та відведення пом'якшеної води: 5 - пробовідбірники; 4 - контактна маса; 6 - скидання повітря; 7 - люк для завантаження контактної маси; 3 – введення реагентів; 2 - видалення відпрацьованої контактної маси
У технологічних схемах реагентного пом'якшення води з освітлювачами замість вихрових реакторів застосовують вертикальні змішувачі (рис. 5). У освітлювачах слід підтримувати постійну температуру, не допускаючи коливань більше 1°С протягом години, оскільки виникають конвекційні струми, змучування осаду та його винесення.
Подібну технологію застосовують для пом'якшення каламутних вод, що містять велику кількість солей магнію. І тут змішувачі завантажують контактної масою. З використанням освітлювачів конструкції Е.Ф. Кургаєва, змішувачі та камери пластівців не передбачають, оскільки змішання реагентів з водою і формування пластівців осаду відбуваються в самих освітлювачах.
Значна висота при невеликому обсязі опадів ущільнювачів дозволяє застосовувати їх для пом'якшення води без підігріву, а також при знекремуванні води каустичним магнезитом. Розподіл вихідної води соплами зумовлює її обертальний рух у нижній частині апарату, що підвищує стійкість завислого шару при коливаннях температури та подачі води. Змішана з реагентами вода проходить горизонтальну та вертикальну змішувальні перегородки та надходить у зону сорбційної сепарації та регулювання структури осаду, що досягається зміною умов відбору осаду по висоті зваженого шару, створюючи передумови для отримання його оптимальної структури, що покращує ефект пом'якшення та освітлення води. Проектують освітлювачі так само, як і для звичайного освітлення води.
При витратах води, що пом'якшується, до 1000 м 3 /добу може бути застосована водоочисна установка типу "Струмінь". Оброблювана вода з доданими до неї реагентами надходить у тонкошаровий відстійник, потім на фільтр.
В Інституті гірничої справи Сибірського відділення РАН розроблено безреагентну електрохімічну технологію пом'якшення води. Використовуючи явище підлужування у анода та підкислення у катода при пропусканні постійного електричного струмучерез водну систему, можна уявити реакцію розряду води наступним рівнянням:
2Н 2 0 + 2е 1 → 20Н - + Н 2,
де е 1 - знак, що вказує на здатність солей жорсткості дисоціювати на катіони Ca(II) та Mg(II).
В результаті протікання цієї реакції концентрація гідроксильних іонів зростає, що викликає зв'язування іонів Mg(II) та Ca(II) у нерозчинні сполуки. З анодної камери діафрагмового (діафрагма з тканини типу бельтинг) електролізера ці іони переходять у катодну за рахунок різниці потенціалів між електродами та наявності електричного поля між ними.
На рис. 6 показано технологічну схему установки для пом'якшення води електрохімічним способом.
Виробнича установка була змонтована у районній котельні, випробування якої тривало близько двох місяців. Режим електрохімічної обробки виявився стійким, осаду в катодних камерах не було.
Напруга на шинах, що підводять, становила 16 В, сумарний струм 1600 А. Загальна продуктивністьустановки - 5 м3/год, швидкість руху води в анодних камерах 0,31 н-0,42 м/хв, зазор між діафрагмою і катодом 0,12-0,18 м/хв.

Рис. 5. Установка звістково-содового пом'якшення води. ,8 - подача вихідної та відведення пом'якшеної води; 2 - ежектор; 3 - бункер із контактною масою; 5 введення реагентів; 6 - Освітлювач з шаром зваженого осаду; 7 - швидкий освітлювальний фільтр; 4 - вихровий реактор

Рис. 6. Схема встановлення електрохімічного пом'якшення води I – випрямляч ВАКГ-3200-18; 2 - діафрагмовий електролізер; 3, 4 - аналіт та каталіт; 5 - Насос; 6 - рН-метр; 7 - освітлювач із шаром зваженого осаду; 8 - освітлювальний швидкий фільтр; 9 - скидання у каналізацію; 10, 11 - відведення пом'якшеної та подача вихідної води; 12 - Витратомір; 13 - витяжна парасолька
Встановлено, що з води з Ж о = 14,5-16,7 мг-екв/л отримують аноліт із твердістю 1,1 - 1,5 мг-екв/л при рН = 2,5-3 та католіт із твердістю 0 6-1 мг-екв/л при рН = 105-11. Після змішування відфільтрованих аноліту та католіту показники пом'якшеної води були наступними: загальна жорсткість Ж о становила 0,8-1,2 мг-екв/л, рН = 8-8,5. Витрати електроенергії становили 3,8 кВт*год/м 3 .
Хімічним, рентгеноструктурним, ІЧ-спектроскопічним та спектральним аналізами встановлено, що в осаді переважно містяться CaC0 3 , Mg (OH) 2 і частково Fe 2 0 3 *Н 2 0. Це свідчить про те, що зв'язування іонів Mg (II) відбувається за рахунок гідроксил-іонів при розряді молекул води на катоді.
Електрохімічна обробка води перед подачею на катіонітові фільтри дозволяє значно (в 15-20 разів) збільшити їхній робочий цикл.
Термохімічний метод пом'якшення води
Термохімічне пом'якшення застосовують виключно при підготовці води для парових казанів,тому що в цьому випадку найбільш раціонально використовується теплота, витрачена на підігрів води. Цим методом пом'якшення води проводять зазвичай при температурі води вище 100 ° С. Більш інтенсивному пом'якшенню води при її підігріві сприяє утворення важких і великих пластівців осаду, швидке його осадження внаслідок зниження в'язкості води при нагріванні, скорочується також витрата вапна, так як вільний оксид вуглецю (IV) видаляється при підігріві до введення реагентів.Термохімічний метод застосовують з додаванням коагулянту і без нього, оскільки велика щільність осаду виключає необхідність у його обтяженні при осадженні. натрію замість вапна дещо спрощує технологію приготування та дозування реагенту, проте економічно така заміна не виправдана через його високу вартість.
Для забезпечення видалення некарбонатної жорсткості води додають соду з надлишком. На рис. 7 показано вплив надлишку соди на залишкову кальцієву та загальну жорсткість води при її термохімічному пом'якшенні. Як видно з графіків, при надлишку соди 0,8 мг-екв/л кальцієва жорсткість може бути знижена до 0,2 а загальна - до 0,23 мг/екв-л. При подальшому додаванні соди жорсткість ще більше знижується. Залишковий вміст магнію у воді може бути знижений до 0,05.0,1 мг-екв/л при надлишку вапна (гідратної лужності) 0,1 мг-екв/л. На рис. 20.8 показано встановлення термохімічного пом'якшення води.
Вапняно-доломитовий методвикористовують для одночасного пом'якшення та знекремування води при температурі 120° С. Цим методом пом'якшення лужність води, обробленої вапном або вапном і содою (без надлишку), може бути знижена до 0,3 мг-екв/л при залишковій концентрації кальцію 1,5 мг -екв/л та до 0,5 мг-екв/л при залишковій концентрації кальцію 0,4 мг-екв/л. Вихідна вода обробляється вапняно-доломитовим молоком і освітлюється в напірному освітлювачі. Потім вона проходить через напірні антрацитові та Na-катіонітові фільтри першого та другого ступенів.
У освітлювачах висоту зони освітлення приймають рівною 1,5 м, швидкість висхідного потоку при вапні - не більше 2 мм/с. Час перебування води в освітлювачі від 0,75 до 1,5 год залежно від виду забруднення, що видаляється. Коагулянт солі заліза (III) рекомендується додавати у кількості 0,4 мг-екв/л.

Рис. 7. Вплив надлишку соди на залишкову кальцієву (а) та загальну (б)жорсткість води при її термохімічному пом'якшенні

Рис. 8. Установка вапняно-содового пом'якшення води з фосфатним пом'якшенням: 1 - скидання шламу з накопичувача 2,3 - Збірник пом'якшеної води; 4 - введення вапна та соди; 5, 11 - подача вихідної та відведення пом'якшеної води; 6 - Введення пари; 7, 8 - термореактор першого та другого ступеня; 9 - Введення тринатрійфосфату; 10 - освітлювальний швидкий фільтр
Метод високотемпературного пом'якшення водизастосовують практично для її повного пом'якшення. Установки термохімічного пом'якшення води зазвичай компактніші. Вони складаються з дозаторів реагентів, підігрівачів тонкошарових відстійників або освітлювачів та фільтрів. Дози вапна Д та і соди Д с, мг/л, при термохімічному пом'якшенні води

де З і З - відповідно вміст СаО і Na 2 C0 3 в технічному продукті, %.
Пом'якшення води діалізом
Діаліз - метод поділу розчинених речовин, що значно відрізняються. молекулярними масами. Він заснований на різних швидкостяхдифузії цих речовин через напівпроникну мембрану, що розділяє концентрований та розбавлений розчини. Під дією градієнта концентрації (за законом діючих мас) розчинені речовини з різними швидкостямидифундують через мембрану у бік розведеного розчину. Розчинник (вода) дифундує у зворотному напрямку, знижуючи швидкість перенесення розчинених речовин. Діаліз здійснюють у мембранних апаратах з нітро- та ацетатцелюлозними плівковими мембранами. Ефективність напівпроникної мембрани для пом'якшення води визначається високими значеннями селективності та водопроникності, які вона повинна зберігати протягом тривалого часу роботи. Селективність мембрани можна виразити так:
(Ж і - Ж у) / Ж і (20.11)
де Ж в - концентрація вихідного розчину(Жорсткість); Жі - жорсткість пом'якшеної води.
Насправді часто використовують коефіцієнт зниження соле - змісту З і /З обр. Він найбільш повно відображає зміни в роботі мембрани, пов'язані з її виготовленням або впливом зовнішніх факторів.
Існує кілька гіпотетичних моделей дії напівпроникних мембран.
Гіпотеза гіперфільтраціїпередбачає існування в напівпроникній мембрані пір, що пропускають при діалізі ас - соціанти молекул води та гідратовані іони солей. Основою теоретичних розробок стало положення про те, що через напівпроникну мембрану вода і розчинені в ній солі проникають за допомогою дифузії та потоків через пори.
Сорбційна модельпроникності заснована на передумові, згідно з якою на поверхні мембрани та її порахадсорбується шар зв'язаної води, що має знижену розчинну здатність. Мембрани будуть напівпроникними, якщо вони, хоча б у поверхневому шарі мають пори, що не перевищують за розміром подвоєної товщини шару зв'язаної рідини.
Дифузійна модельвиходить із припущення, що компоненти системи розчиняються у матеріалі мембрани та дифундують через неї. Селективність мембрани пояснюється різницею в коефіцієнтах дифузії та розчинності компонентів системи у її матеріалі.
Електростатична теоріяполягає в наступному. При русі вихідної води в камері з одного боку селективної (катіонітової) мембрани, а розсолу з іншого, іони натрію у разі, коли розсіл приготований з розчину кухонної солі, мігрують в мембрану і далі вихідну воду, а іони кальцію в протилежному напрямку, тобто. з твердої води в розсіл. Таким чином, відбувається видалення іонів кальцію з вихідної води та заміна їх неосадкоутворюючими іонами натрію. Одночасно в камерах відбуваються побічні процеси, що супроводжують основний процес діалізу: осмотичні переноси води, перенесення однойменних іонів, дифузія електроліту. Ці процеси залежить від якості мембрани.
Рівняння обміну між іонами, що містяться у вихідній воді, та іонами в мембрані має вигляд
де х, х- інші іони, що містяться в розчині та в мембрані.
Константа рівноваги
![]()
Рівняння обміну написано тільки для іона кальцію, але фактично необхідно враховувати суму іонів кальцію і магнію. Рівновага між розсолом і мембраною має вигляд:

Якщо k1+ k 2 то
![]()
де n - показник ступеня, що залежить від того, які іони входять до складу розчину.
З останнього виразу можна зробити висновок, що, якщо рівновазі відношення іонів натрію в розсолі і жорсткій вихідній воді дорівнює, наприклад, 10, то жорсткість у вихідній воді буде приблизно в 100 разів менше, ніж у розсолі. Площа, м 2 , поверхні мембрани
де М - кількість речовини, що пройшла через мембрану; ΔС ср - рушійна сила процесу, тобто різниця концентрацій речовини по обидві сторони мембрани; К д - коефіцієнт масопередачі, що визначається зазвичай експериментально або приблизно з виразу
![]()
β 1 і β 2 - відповідні коефіцієнти швидкості перенесення речовини в концентрованому розчині до мембрани та від неї в розведеному; б – товщина мембрани; D- Коефіцієнт дифузії розчиненої речовини.
Жорсткість пом'якшеної води після діалізу:

де С д і С р - концентрації солей на початку апарату відповідно в діалізаті та в розсолі, мг-екв/л; і Q p - продуктивність апарату відповідно по діалізату та розсолу, м 3 /год; Ж д і Ж р - жорсткість діалізату та розсолу на початку апарату, мг-екв/л; а - константа, яка визначається властивостями мембран і розчинів; L- Довжина шляху розчину в діалізатній та розсольній камерах апарату, м; ? д - швидкість руху діалізату в камері, м/с.
Експериментальна перевірка рівняння (20.13) на катіонітових мембранах МКК показала хорошу збіжність результатів. Аналіз формули (20.13) показує, що зменшення швидкості руху діалізату в камерах апарату збільшує ефект пом'якшення, зниження жорсткості пом'якшеної води прямо пропорційно концентрації розсолу.
Магнітна обробка води
У Останнім часому вітчизняній та зарубіжній практиці для боротьби з накипівтворенням та інкрустацією успішно застосовують магнітну обробку води. Механізм впливу магнітного поля на водута її домішки остаточно не з'ясовано, є низка гіпотез, які Є.Ф. Тебенихіним класифіковані на три групи: перша, що поєднує більшість гіпотез, пов'язує дію магнітного поля на іони солей, розчинених у воді. Під впливом магнітного полявідбуваються поляризація та деформація іонів, що супроводжуються зменшенням їх гідратації, що підвищує ймовірність їх зближення, та зрештою освітацентрів кристалізації; друга передбачає дію магнітного поля на колоїдні домішки води; третя група поєднує уявлення про можливий вплив магнітного поля на структуру води. Цевплив, з одного боку, може спричинити зміни в агрегації молекул води, з іншого – порушити орієнтацію ядерних спинів водню у її молекулах.
Обробка води в магнітному полі поширена для боротьби з накипівтворенням.Сутність методу полягає в тому, що при перетині магнітною водою силових лінійнакипеобразователи виділяються не так на поверхні нагріву, а масі води. Пухкі опади (шлам), що утворюються, видаляють при продуванні. Метод ефективний при обробці вод кальцієво-карбонатного класу, які становлять близько 80% вод усіх водойм нашої країни та охоплюють приблизно 85% її території.
Обробка води магнітним полем отримала широке застосуваннядля боротьби з накипеутворенням у конденсаторах парових турбін, у парогенераторах низького тиску та малої продуктивності, у теплових мережах та мережах гарячого водопостачання та різних теплообмінних апаратах, де застосування інших методів обробки води економічно недоцільне. У порівнянні з пом'якшенням води основними перевагами її магнітної обробки є простота, дешевизна, безпека та майже повна відсутність експлуатаційних витрат.
Магнітна обробка природних вод (як прісних, так і мінералізованих) призводить до зменшення інтенсивності утворення накипу на поверхнях нагріву лише за умови перенасиченості їх як карбонатом, так і сульфатом кальцію в момент впливу магнітного поля та за умови, що концентрація вільного оксиду вуглецю (IV) менше його рівноважної концентрації. Протинакіпний ефект Е обумовлює присутність у воді оксидів заліза та інших домішок:
де m н і m м - маса накипу, що утворилася на поверхні нагріву при кип'ятінні в однакових умовах однієї й тієї ж кількості води, відповідно необробленої та обробленої магнітним полем, г.
Протинакіпний ефект залежить від складу води, напруженості магнітного поля, швидкості руху води та тривалості її перебування в магнітному полі та інших факторів. На практиці застосовують магнітні апарати з постійними сталевими або ферито-барієвими магнітами та електромагнітами (рис. 9). Апарати з постійними магнітами конструктивно простіші і не вимагають живлення від електромережі. В апаратах з електромагнітом на сердечник (керн) намотуються котушки дроту, що утворюють магнітне поле.
Магнітний апарат монтується до трубопроводів у вертикальному або горизонтальному положенні за допомогою перехідних муфт. Швидкість руху води у зазорі має перевищувати 1 м/с. Процес роботи апаратів може супроводжуватися забрудненням прохідного зазору механічними головним чином феромагнітними домішками. Тому апарати з постійними магнітами необхідно періодично розбирати та чистити. Оксиди заліза з апаратів з електромагнітними видаляють відключивши їх від мережі.
Результати досліджень МДСУ (Г.І. Ніколадзе, В.Б. Вікуліна) показали, що для води з карбонатною жорсткістю 6.7 мкг-екв/л, окислюваністю 5,6 мг02/л і солевмістом 385.420 мг/л, оптимальна напруженість магнітного поля становила (10.12,8) * 19 4 А/м, що відповідає силі струму 7.8 А.
Схему установки для магнітної обробки додаткової живильної води опалювальних парових котлів наведено на рис. 20.10.
Останнім часом набули поширення апарати із зовнішніми намагнічуючими котушками. Для омагнічування великих мас води створено апарати з пошаровою обробкою.
Крім запобігання накипу утворення магнітна обробка , за даними П.П. Строкача може застосовуватися для інтенсифікації процесу коагуляції та кристалізації, прискорення розчинення реагентів, підвищення ефективності використання іонообмінних смол, поліпшення бактерицидної дії дезінфектантів.

Рис. 9. Електромагнітний апарат для протинакипної обробки води ВКВ ОТІ: 1,8 - подача вихідної та відведення омагніченої води; 2 - Сітка; 3 - робочий зазор для проходу води, що омагнічується; 4 - кожух; 5 - котушка, що намагнічує; 6 - сердечник; 7 - Корпус; 9 - кришка; 10 – клеми
p align="justify"> При проектуванні магнітних апаратів для обробки води задаються такі дані: тип апарату, його продуктивність, індукція магнітного поля в робочому зазорі або відповідна їй напруженість магнітного поля, швидкість води в робочому зазорі, час проходження водою активної зони апарату, рід і його напруга для електромагнітного апарату або магнітний сплав та розміри магніту для апаратів з постійними магнітами.

Рис. 10. Схема розміщення магнітної установки для обробки котлової води без попереднього очищення.
1,8 - вихідна та підживлювальна вода; 2 - Електромагнітні апарати; 3, 4 - підігрівачі І та ІІ ступенів; 5 - Деаератор; 6 - проміжний бак; 7 - підживлювальний насос
Література
1. Алексєєв Л.С., Гладков В.А. Поліпшення якості м'яких вод. М.,
2. Будвидав, 1994 р.
3. Алфьорова Л.А., Нечаєв А.П. Замкнуті системиводного господарства промислових підприємств, комплексів та районів. М., 1984.
4. Аюкаєв Р.І., Мельцер В.З. Виробництво та застосування фільтруючих матеріалів для очищення води.Л., 1985.
5. Вейцер Ю.М., Мііц Д.М. Високомолекулярні флокулянти у процесах очищення води. М., 1984.
6. Єгоров А.І. Гідравліка напірних трубчастих систем у водопровідних очисних спорудах. М., 1984.
7. Журба М.Г. Очищення води на зернистих фільтрах. Львів, 1980.
Однією з проблем, які важко вирішувати, на сьогодні є погана вода. Масове її використання має на увазі обов'язкове використання води хорошої якості, але в реаліях, на кухнях і у ванних кімнатах застосовується вода зовсім іншої якості. Централізована системаочищення води постачає на підприємства і для приватного використання воду з високим порогом жорсткості.
Що робити з вапном?
Отже, є вихідні дані. До будинку, квартири надходить вода низької якості. Тут же споживач може заперечити, що неякісної води не може бути. Її допустили згідно з ГОСТами та СанПіном до використання, і отже якась там жорсткість є чи не міфом. Та при роботі з такою водою утворюється шкідливий наліт. Але його цілком можна усунути самотужки, шляхом звичайних чисток. На підприємствах неефективні обертаються у великі статті видатків і там ця логіка не працює.
При цьому жорсткість, як перевищення певної норми вмісту кальцію і магнію у воді, точніше їх солей, може бути різною. І шкода від такої води теж відрізнятиметься. Поділ за видами вапняності представлений у таблиці.
Все, що понад показник сімки може приносити шкоду і не малий. Способи пом'якшення водина такі випадки таки розроблялися.
До основних негативних наслідківжорсткості відносяться:
- Різке зростання витрат палива та миючих засобіві самої води;
- Освіта блокуючої тепло, накипу;
- Поломки обладнання;
- Негативний вплив на якість прання
Чи можна сплутати роботу жорсткості з іншими домішками? на початкових стадіях, Поки накипу ще немає або вона дуже тонка, можна. Поки щільний осад утворюється, вапняність можна прийняти за достаток хлорки у питній воді.
На великих промислових підприємствах, де виробляють питну воду чи працюють із водою постійно, жорсткість поводиться відразу. Є правила, які не можна порушувати. Т.к. шар накипу в казані не повинен перевищувати якихось півміліметра. Звідки такі обмеження? Усе це безпосередньо з особливостями вапняності, як матеріалу.
Коли вона осідає на поверхню, передача тепла у воду практично припиняється. Вапно працює як ефективний блокатор. І чим вона щільніша, тим гірша передача тепла. Коли накип сягає стану гіпсу, передача тепла припиняється майже повністю. Щоправда, нагрівальний елемент у цьому випадку перегорить раніше. Аспект у тому, що енергія з металу нікуди не йде, вона продовжує його розжарювати доти, доки він не видозміниться. Тобто або вибухне, або розплавиться. У галузях з таких наслідків і починали довгий шлях пошуків відповідних способів пом'якшення води.
Уникнути всього цього букета можна, як відомо, шляхом постійних чисток та промивок, або шляхом розробки та монтажу очисної системи. Перший варіант вирішення проблеми досі застосовують, але тільки там, де поки що немає можливості встановити прогресивне пом'якшувальне обладнання, або хоча б просто пом'якшувальне обладнання.
Чищення поверхонь мають велику популярність у населення. Точніше, навіть у тих верств, хто ними власне не займається, але вважає, що вони явно дешевші двох пом'якшуючих приладів у квартиру. Але будь-яка чистка залишить після себе сліди. І щітка, і кислота відчищають разом із накипом та поверхні. Через це обладнання служитиме менше, а чищення надалі тільки почастішають.
Причому на підприємстві такі чистки виглядають як профілактичні та капітальні. Останні проводяться не частіше за два рази за весь час роботи обладнання. Таке капітальне чищення має на увазі повне розбиранняобладнання. Особливо забруднені поверхні замочують у кислотних розчинах, там розпушуються старі залишки і лише потім виробляють механічне очищення. Причому етап замочування може тривати кілька годин. Такі розбирання означають простої і спричиняють упущену вигоду. Із застосуванням пом'якшувальних установок, капітальні чисткийдуть у минуле. Навіть при сильно жорсткій воді, достатньо прополоскати систему зворотним протоком води, щоб винести легкі суспензії, на які перетворюються солі жорсткості.
Способи пом'якшення жорсткої води – інструкція із застосування
Щоб не витрачати величезні кошти на очищення, не закуповувати постійно розчини для пом'якшення води або усунення накипу, було створено різні ефективні та не ефективні способи пом'якшення жорсткої води. Їхнє завдання по-різному, але позбавити воду від надлишків солей жорсткості. Якщо їх усунути, то накипні відкладення у воді не утворюватимуться.
Зробити це можна за допомогою двох напрямів. Можна воду пом'якшувати, шляхом додавання до неї якихось спеціальних засобів, що пом'якшують, можна воду опромінювати. За цим принципом і всі установки, що пом'якшують, сьогодні діляться. Хочеш отримати м'яку воду, створи якусь нову речовину, яка не осяде на поверхні і легко відфільтрується, або впливай на воду, якоюсь природною силою.
Реагентні пом'якшувачі загалом поділяються на два види. Це дезінфектори, сильно схожі на дезінфектори для знезараження, і катіонні пом'якшувачі. Перші працюють за найпростішим принципом – додаємо у воду пом'якшувач, вона стає м'якшою.
Другі працюють на обмінному процесі. Заповнюють обмінний картридж катіонною смолою. Слід розглянути, до чого дуже ефективний. У ній велика кількість натрію. При контакті із солями жорсткості, натрій та солі змінюються місцями. Споживачу надходить вже пом'якшена вода. Але картридж досить швидко прийде в непридатність. Натрій весь вимиється, і його потрібно буде міняти. У промислових виробничих процесівкартриджі відновлюють за допомогою промивання сильно соляним розчином. При особистому споживанні та виробництві питної води картридж змінюють.
Коли його відновлюють, утворюються дуже шкідливі відходи, які мало того, що потрібно почистити, потрібно ще й дозвіл отримати на те, щоб їх злити в атмосферу. Та й самі картриджі згодом доведеться міняти. Таке пом'якшення при первинних малих вкладеннях, надалі виявляється недешевим. Але гарантує гарна якістьбезпосередньо пом'якшення. Та й для підвищення якості пом'якшення, воду можна прогнати через установку ще раз.
Дезінфектор передбачає просте впорскування у воду спеціальних речовин, що пом'якшують воду. Такий прилад врізається у трубу. Є у нього блок управління, де задається частота, час і об'єм подачі пом'якшувальних засобів. Тут постійно вимірюють електропровідність води, з метою зрозуміти жорстка вода чи ні. Контроль триває постійно. Так вплив людського факторазнижується та значно.
Друга група ефективних способівпом'якшення жорсткої води відноситься до безреагентним. Яскраві представники від магніту до електричних імпульсів. Найбільше сьогодні застосовують електромагніти. Маленькі безпроблемні гарантують не тільки м'яку воду в системі. З їхньою допомогою можна позбутися старих накипних слідів у будь-якому місці системи, зовсім не розбираючи установки. Причому працювати прилад буде економно, всього якихось п'ять кіловат на місяць електроенергії. Змінних картриджів немає, стежити за станом та оновленням не потрібно. Щоправда якість питної води такий прилад не дає, але для обслуговування всієї води в квартирі або котельні, наприклад, просто незамінний.
Обмеження в його роботі деякі все ж таки є. Він не працює з водою без руху та не дає питної якості. Його ефект не тримається довгий час.
Ще одна група ефективних способів пом'якшення твердої води відноситься до тонкому очищенню. Такі прилади усувають із води майже всі домішки органічного характеру. До них відноситься ультрафільтрація, Зворотній осмос, нанофільтрація. Основний удар у таких системах приймає він мембрана. Вона найдорожча у приладі та найсприйнятливіша. Без підготовки воду через неї пропускати не можна. Звідси й дорожнеча. Правда, такі пристрої часто занадто багато прибирають із води, що так само обмежує, але не сильно їх застосування.
Технологічні схеми та конструктивні елементи установок реагентного пом'якшення води
Термохімічний метод пом'якшення води
Пом'якшення води діалізом
Магнітна обробка води
Література
Теоретичні основи пом'якшення води, класифікація методів
Під пом'якшенням води мається на увазі процес видалення із неї катіонів жорсткості, тобто. кальцію та магнію.Відповідно до ГОСТ 2874-82 "Вода питна" жорсткість води не повинна перевищувати 7 мг-екв/л. Окремі види виробництв до технологічної води висувають вимоги глибокого її пом'якшення, тобто. до 0,05.0,01 мг-екв/л. Зазвичай використовувані вододжерела мають жорсткість, що відповідає нормам господарсько-питних вод, і пом'якшення не потребують. Пом'якшення води виробляють в основному під час її підготовки для технічних цілей. Так, жорсткість води для живлення барабанних котлів має перевищувати 0,005 мг-экв/л. Пом'якшення води здійснюють методами: термічним, заснованим на нагріванні води, її дистиляції або виморожуванні; реагентними, при яких іони, що знаходяться у воді Ca ( II ) та Mg ( II ) пов'язують різними реагентами практично нерозчинні сполуки; іонного обміну, заснованого на фільтруванні пом'якшувальної води через спеціальні матеріали, що обмінюють іони, що входять до їх складу. Na ( I) або Н (1) на іони Са (II) та Mg ( II ), що містяться у воді діалізу; комбінованим, що є різними поєднаннями перерахованих методів.
Вибір методу пом'якшення води визначається її якістю, необхідною глибиною пом'якшення та техніко-економічними міркуваннями. Відповідно до рекомендацій СНіПу при пом'якшенні підземних вод слід застосовувати іонообмінні методи; при пом'якшенні поверхневих вод, коли одночасно потрібне і освітлення води, - вапняний або вапняно-содовий метод, а при глибокому пом'якшенні води - подальше катіонування.Основні характеристики та умови застосування методів пом'якшення води наведено у табл. 20.1.
пом'якшення вода діаліз термічний
Для отримання води для господарсько-питних потреб зазвичай пом'якшують лише її деяку частину з наступним змішуванням з вихідною водою, при цьому кількість води, що пом'якшується. Q yвизначають за формулою
(20.1)де Ж о. в. - загальна жорсткість вихідної води, мг-екв/л; Ж 0. с. - загальна жорсткість води, що надходить до мережі, мг-екв/л; Ж 0.у. - Жорсткість пом'якшеної води, мг-екв/л.
Методи пом'якшення води
| Показник | термічний | реагентний | іонообмінний | діалізу |
| Характеристика процесу | Воду нагрівають до температури вище 100°С, при цьому видаляється карбонатна і некарбонатна жорсткості (у вигляді карбонату кальцію, гідрокси- та магнію і гіпсу). | У воду додають вапно, що усуває карбонатну і магнієву жорсткість, а також соду, що усуває некарбонат - іншу жорсткість | Пом'якшувальна вода пропускається через катіонітові фільтри | Вихідна вода фільтрується через напівпроникну мембрану |
| Призначення методу | Усунення карбонатної жорсткості з води, що використовується для живлення котлів низького н середнього тиску | Неглибоке пом'якшення при одночасному освітленні води від завислих речовин | Глибоке пом'якшення води, що містить незначну кількість завислих речовин | Глибоке пом'якшення води |
| Витрата води на власні потреби | - | Не більше 10% | До 30% і більше пропорційно жорсткості вихідної води | 10 |
| Умови ефективного застосування: каламутність вихідної води, мг/л | До 50 | До 500 | Не більше 8 | До 2,0 |
| Жорсткість води, мг-екв/л | Карбонатна жорсткість з переважанням Са (НС03) 2, некарбонатна жорсткість у вигляді гіпсу | 5.30 | Не вище 15 | До 10,0 |
| Залишкова жорсткість води, мг-екв/л | Карбонатна жорсткість до 0,035, CaS04 до 0,70 | До 0,70 | 0,03.0,05 прн одноступінчастому і до 0,01 при двоступінчастому катіонуванні | 0,01 і нижче |
| Температура води, ° С | До 270 | До 90 | До 30 (глауконіт), до 60 (сульфовугілля) | До 60 |
Термічний метод пом'якшення води
Термічний метод пом'якшення води доцільно застосовувати під час використання карбонатних вод, що йдуть харчування котлів низького тиску, і навіть у поєднанні з реагентними методами пом'якшення води. Він заснований на усуненні вуглекислотної рівноваги при її нагріванні у бік утворення карбонату кальцію, що описується реакцією
Са (НС0 3) 2 -> СаСО 3 + С0 2 + Н 20.
Рівнавага зміщується за рахунок зниження розчинності оксиду вуглецю (IV), що викликається підвищенням температури та тиску. Кип'ятінням можна повністю видалити оксид вуглецю (IV) і цим значно знизити карбонатну кальцієву жорсткість. Однак, повністю усунути зазначену жорсткість не вдається, оскільки карбонат кальцію хоча і незначно (13 мг/л при температурі 18°С), але все ж таки розчинний у воді.
За наявності у воді гідрокарбонату магнію процес його осадження відбувається так: спочатку утворюється порівняно добре розчинний (110 мг/л при температурі 18° С) карбонат магнію
Mg (НСО 3) → MgC0 3 + С0 2 + Н 2 0,
який при тривалому кип'ятінні гідролізується, внаслідок чого випадає осад малорозчинного (8,4 мг/л). гідроксиду магнію
MgC0 3 +H 2 0 → Mg (0H) 2 +C0 2 .
Отже, при кип'ятінні води жорсткість, що обумовлюється гідрокарбонатами кальцію та магнію, знижується. При кип'ятінні води знижується також жорсткість, яка визначається сульфатом кальцію, розчинність якого падає до 0,65 г/л.
На рис. 1 показаний термопом'якшувач конструкції Коп'єва, що відрізняється відносною простотою пристрою та надійністю роботи. Попередньо підігріта в апараті вода, що обробляється, надходить через ежектор на розетку плівкового підігрівача і розбризкується над вертикально розміщеними трубами, і по них стікає вниз назустріч гарячій парі. Потім разом з продувною водою від котлів вона по трубі, що центрально подає, через дірчасте днище надходить у освітлювач зі зваженим осадом.
Вуглекислота, що виділяється при цьому з води, і кисень разом з надлишком пари скидаються в атмосферу. Солі кальцію і магнію, що утворюються в процесі нагрівання води, затримуються у зваженому шарі. Пройшовши через зважений шар, пом'якшена вода надходить до збірки та відводиться за межі апарату.
Час перебування води в термопом'якшувачі становить 30.45 хв, швидкість її висхідного руху у завислому шарі 7.10 м/год, а в отворах хибного дна 0,1.0,25 м/с.

Рис. 1. Термопом'якшувач конструкції Коп'єва.
15 - скидання дренажної води; 12 - центральна труба, що подає; 13 - хибні перфоровані днища; 11 - зважений шар; 14 - скидання шламу; 9 - збірка пом'якшеної води; 1, 10 - подача вихідної та відведення пом'якшеної води; 2 - продування котлів; 3 - ежектор; 4 - Випар; 5 - плівковий підігрівач; 6 - скидання пари; 7 - кільцевий перфорований трубопровід відведення води до ежектора; 8 - похилі перегородки, що сепарують.
Реагентні методи пом'якшення води
Пом'якшення води реагентними методами засноване на обробці її реагентами, що утворюють з кальцієм і магнієм малорозчинні сполуки: Mg (OH) 2 , СаС0 3 Са 3 (Р0 4) 2 , Mg 3 (P0 4) 2 та інші з подальшим їх відділенням в освітлювачах , тонкошарових відстійниках та освітлювальних фільтрах. Як реагентів використовують вапно, кальциновану соду, гідроксиди натрію та барію та інші речовини.
Пом'якшення води вапнуваннямзастосовують при її високій карбонатній та низькій некарботаній жорсткості, а також у разі, коли не потрібно видаляти з води солі некарбонатної жорсткості. Як реагент використовують вапно, яке вводять у вигляді розчину або суспензії (молоку) попередньо підігріту оброблювану воду. Розчиняючись, вапно збагачує воду іонами ОН - і Са 2+ , що призводить до зв'язування розчиненого у воді вільного оксиду вуглецю (IV) з утворенням карбонатних іонів та переходу гідрокарбонатних іонів у карбонатні:
С0 2 + 20Н - → ЗІ 3 + Н 2 0, НСО 3 - + ВІН - → ЗІ 3 - + Н 2 О.
Підвищення в оброблюваній воді концентрації іонів С0 3 2 - і присутність у ній іонів Са 2+ з урахуванням введених з вапном призводить до підвищення твору розчинності та осадження малорозчинного карбонату кальцію:
Са 2+ С0 3 - → СаС0 3 .
При надлишку вапна в осад випадає і гідроксид магнію
Mg 2+ + 20Н - → Mg (ОН) 2
Для прискорення видалення дисперсних та колоїдних домішок та зниження лужності води одночасно з вапнуванням застосовують коагуляцію цих домішок сульфатом заліза (II), тобто. FeS0 4 *7 Н 2 0. Залишкова жорсткість пом'якшеної води при декарбонізації може бути отримана на 0,4.0,8 мг-екв/л більше некарбонатної жорсткості, а лужність 0,8.1,2 мг-екв/л. Доза вапна визначається співвідношенням концентрації у воді іонів кальцію та карбонатної жорсткості: а) при співвідношенні [Са 2+] /20<Ж к,
(20.2б)б) при співвідношенні [Са 2+] /20 > Ж к,
(20.3)де [СО 2 ] - Концентрація у воді вільного оксиду вуглецю (IV), мг/л; [Са 2+] - концентрація іонів кальцію, мг/л; Ж к - карбонатна жорсткість води, мг-екв/л; Д до - доза коагулянту (FeS0 4 або FeCl 3 у перерахунку на безводні продукти), мг/л; е до- еквівалентна маса активної речовини коагулянту, мг/мг-екв (для FeS0 4 едо = 76, для FeCl 3 е к = 54); 0,5 і 0,3 - надлишок вапна для забезпечення більшої повноти реакції, мг-екв/л.
Існує поширена думка, що воду з глибинних водоносних шарів можна вживати в їжу без попередньої підготовки. Дійсно, вода з них набагато чистіша, ніж з верховодки, проте, і в ній є домішки, наявність яких може негативно позначитися на здоров'ї людини та роботі обладнання. Щоб докладно розібратися у питанні, звернімося до фахівців відділу систем водоочищення компанії БІІКС.
Вода – це чудовий розчинник. Перебуваючи у постійному контакті з гірськими породами, вона насичується речовинами, у тому числі ці породи складаються. Згодом накопичується величезна кількість сполук. Склад води залежить від типу породи, де проходить водоносний шар. Для Москви та Підмосков'я характерний високий вміст карбонатних солей жорсткості та сполук заліза.
Тривале вживання в їжу води підвищеної жорсткості призводить до відкладень конкрементів у нирках (каменів), при контакті шкіра та волосся стає сухим. Під час нагрівання з'єднання випадають в осад, утворюючи твердий, наліт, що погано видаляється. Стають непридатними ТЕНи, засмічуються труби і шланги, підвищується швидкість зносу рухомих частин устаткування.

Перевищення жорсткості може бути:
- візуально: утворення нальоту на сантехніці та нагрівальних елементах (в чайнику, на ТЕНах пральних та посудомийних машин, бойлерів);
- на смак: у порівнянні з бутильованою водою відомої жорсткості;
- з піноутворення: у твердій воді утворюється менше піни і витрата миючих засобів вище;
- в лабораторії.
Пом'якшення води - це зниження концентрації солей жорсткості та приведення цих показників до рекомендованих значень.
Норми жорсткості води
Залежно від концентрації солей жорсткості воду ділять на:
- м'яку - вміст солей трохи більше 2 мг-экв/л;
- нормальну - вміст солей у межах 2 - 4 мг-екв/л;
- жорстку - вміст солей у межах 4 - 6 мг-екв/л;
- високої жорсткості – вміст солей вище 6 мг-екв/л.
Російським стандартом, що регламентує якість питної води, встановлено граничне значення концентрації солей жорсткості лише на рівні 7,0 мг-экв/л. Тоді як ВООЗ встановлює цей показник лише на рівні 2,5 мг-экв/л, а ЄЕС прийнято норматив 2,9 мг-экв/л. Таким чином, як питна водопровідна вода в Росії допустима подача дуже жорсткої води, з дворазовим перевищенням рекомендацій ВООЗ.
Способи пом'якшення води
Термічний

Іншими словами – кип'ятіння. При підвищенні температури розчинний гідрокарбонат кальцію (найпоширеніша сполука, що викликає жорсткість) розпадається на нерозчинний карбонат кальцію і вуглекислий газ. Нерозчинна частина випадає в осад, газ випаровується. Частково при кип'ятінні зменшується концентрація та сульфату кальцію. Термічний спосіб найдоступніший у побутових умовах, але не найзручніший і має низьку продуктивність. Крім того, він не підходить для сполук магнію.
Мембранний

Для пом'якшення води у такий спосіб використовуються молекулярні мембрани, які пропускають лише частинки води, видаляючи більшу частину домішок (до 98%). Так діють фільтри зворотного осмосу.
Не треба пити забруднену воду заради деяких нібито корисних солей, які в ній також містяться. Набагато краще живити свій організм тими самими речовинами, але які у звичайних продуктах. Власне, людство все своє життя і бере їх саме у хлібі, молоці, м'ясі, рибі, овочах та фруктах. Наприклад, у склянці молока лише кальцію в сотні разів більше, ніж у склянці водопровідної. У деяких випадках для підготовки питної води в такий спосіб встановлюється мінералізатор.
Хімічний (реагентний)

Суть способу - перетворити розчинні сполуки на нерозчинні. Для цього використовуються різні реактиви, залежно від переважання у воді солей того чи іншого типу. Для солей карбонатного типу використовується вапно, сполуки натрію, сода та синтетичні сполуки, наприклад, тринатрійфосфат. У результаті вода пом'якшується, але через наявність реагентів у їжу вживати її не можна.
Магнітний

На воду впливають наведенням постійного магнітного поля. Проходження через магнітне поле змінює структуру солей жорсткості. Молекули перестають з'єднуватися при нагріванні і не утворюють осад, а також розпушують шар вже наявного накипу, який розчиняється у воді. Такий метод не знижує концентрацію солей, а перешкоджає їхньому відкладенню у вигляді осаду. Для побутових цілей така вода підходить добре: труби, насосне обладнаннята нагрівальні елементи прослужать довше. Ефективно пом'якшувати воду можна за допомогою магнітів можна тільки в невеликих обсягах та швидкості потоку не вище 0,5 м/с. За допомогою магнітного пом'якшувача також знижується вміст заліза.
Електромагнітний

Є вдосконаленою версією магнітного з тією різницею, що надлишок солей не тільки втрачає здатність випадати у вигляді осаду, але й видаляється через відстійник у каналізацію.
Іонообмінний
Суть методу полягає в заміщенні іонів кальцію та магнію на іони натрію, сполуки якого розчиняються і не надають негативного впливуна здоров'я та обладнання.
Сучасні системи очищення питної води часто поєднують кілька методів, які залежать від аналізу води зі свердловини. Визначити, який тип пом'якшувача потрібен у вашій ситуації, допоможуть фахівці з водоочищення. Для артезіанських свердловин біля Підмосков'я, де переважають карбонати, рекомендується встановлення пом'якшувачів води іонообмінного типу.

Конструктивно пристрій є пластиковим балоном, всередину якого у вигляді гранул засипається полімерна іонообмінна смола, здатна віддавати іони натрію і поглинати іони кальцію і магнію. Вода, що надходить у балон, повільно проходить крізь смолу, на якій відбувається реакція заміщення. Коли концентрація іонів натрію в смолі падає, необхідно провести процес промивки та регенерації. З балоном цих цілей з'єднаний сольовий бачок, звідки надходить розчин хлориду натрію. Процес контролюється автоматичним блоком керування. Під час промивання подача пом'якшеної води припиняється, тому регенерація програмується на нічний час. Якщо аналіз води відбувається безперервно, то рекомендується встановлювати два балони і запускати регенерацію по черзі. Періодично, у середньому через 3-4 роки, смолу необхідно міняти, оскільки кількість циклів її відновлення обмежена. Продуктивність системи залежить від обсягу завантаження балона.
Стаття підготовлена за участю фахівців відділу систем водоочищення